
Wetenschap
Hoe neutronen, protonen en elektronen in atomen, ionen en isotopen te bepalen
Door Riti Gupta – Bijgewerkt op 24 maart 2022
Wanneer u de subatomaire samenstelling van een chemische soort moet identificeren, is het periodiek systeem uw primaire referentie. Hieronder vindt u een duidelijke handleiding over hoe u het aantal neutronen, protonen en elektronen voor neutrale atomen, geladen ionen en isotopen kunt extraheren met behulp van het periodiek systeem en de nucleaire notatie.
Het periodiek systeem lezen
Het periodiek systeem bevat alle informatie die u nodig heeft over de subatomaire structuur van een element:
- Symbool – De elementaire afkorting (bijvoorbeeld C voor koolstof).
- Atoomnummer (Z) – Gelegen boven het symbool, is het gelijk aan het aantal protonen en, voor een neutraal atoom, aan het aantal elektronen. Voor koolstof,
Z = 6. - Atoommassa – Onder het symbool een gewogen gemiddelde van alle natuurlijke isotopen. Wanneer het wordt afgerond op het dichtstbijzijnde gehele getal, komt het overeen met het massagetal van de meest voorkomende isotoop. Voor koolstof levert dit een massagetal
M = 12op , wat de som is van protonen en neutronen.
Om het aantal neutronen in een neutraal atoom te vinden, trekt u het atoomnummer af van het massagetal:
#neutrons = M – Z – Voor koolstof, 12 – 6 = 6 neutronen.
Subatomaire deeltjes in ionen berekenen
Ionen ontstaan wanneer een atoom elektronen wint of verliest, waardoor de algehele lading verandert. Het superscript op het ionensymbool geeft de nettolading aan. Bijvoorbeeld Cl – is een chloride-ion met een lading van -1.
Bepaal eerst het aantal protonen en neutronen van het neutrale atoom uit het periodiek systeem. Chloor heeft Z = 17 protonen en, met behulp van M = 35 , #neutrons = 35 – 17 = 18 neutronen.
Omdat het ion een negatieve lading heeft, bevat het één extra elektron. Gebruik de ladingsbalansvergelijking:
#e– + #p+ = charge
Vervanging van de bekende waarden voor chloride:
#e– + 17 = –1 → #e– = 18
Dus Cl – bevat 17 protonen, 18 neutronen en 18 elektronen.
Identificeren van subatomaire deeltjes in isotopen
Isotopen zijn varianten van hetzelfde element die alleen verschillen in het aantal neutronen. Nucleaire notatie is een beknopte manier om ze weer te geven. Koolstof‑12 wordt bijvoorbeeld geschreven als ¹²⁶C .
In nucleaire notatie:
- Symbool – Het symbool van het element (C).
- Massagetal (A) – Het superscript (12) is gelijk aan protonen + neutronen.
- Atoomnummer (Z) – Het subscript (6) is het aantal protonen, constant voor het element.
Om het aantal neutronen voor een specifieke isotoop te vinden, los je het volgende op:
#neutrons + Z = A
Voor koolstof‑13 (¹³⁶C ):
#neutrons + 6 = 13 → #neutrons = 7
Daarom heeft koolstof-13 6 protonen, 7 neutronen en, indien neutraal, 6 elektronen. Koolstof-12 heeft 6 protonen, 6 neutronen en 6 elektronen.
Door periodieke tabelgegevens te combineren met nucleaire notatie, kunt u nauwkeurig de subatomaire samenstelling van elk atoom, ion of isotoop bepalen.
Hoofdlijnen
- Als een voedingsstof schaars een ecosysteem heeft, hoe zal deze dan het organisme beïnvloeden?
- Schimmelresistentie bij planten geassocieerd met erfelijke verschillen in de overvloed aan microbiota
- Wat wordt bedoeld met monosporische ontwikkeling van vrouwelijke gametofyt?
- Wat produceert cellulaire ademhaling en wat is de reden daarvoor?
- Hoe wordt voorkomen dat HIV-DNA de celkern binnendringt
- Waarom worden planten geclassificeerd?
- Welke structuren in amoeba en paramecium komen ook op plantencellen?
- Wat zijn twee voorbeelden van celspecialisaties die bij mensen worden gevonden, vermelden hun functies?
- Welke factoren beïnvloeden het overleven en verandering van een soort in de loop van de tijd?
- Ontdekking daagt geaccepteerde regel van organisch zonnecelontwerp uit

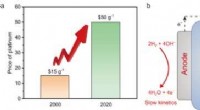
- Goedkope legering concurreert met duur platina om brandstofcellen te stimuleren
- Succesvolle synthese van nanomateriaal dat de efficiëntie van de katalysator verbetert

- Hondenvoer verrukkelijker maken door aroma's te analyseren

- Team verlicht de micro-omgeving, een nieuwe weg naar kankermedicijnen creëren
 Welke transformatie van energie gebeurt in rollend speelgoed?
Welke transformatie van energie gebeurt in rollend speelgoed?  Vaste stikstof:conversieproces en methoden
Vaste stikstof:conversieproces en methoden  Welk gas dat wordt vrijgegeven uit brandende brandstoffen is in de grootste hoeveelheid en draagt bij aan de opwarming van de aarde?
Welk gas dat wordt vrijgegeven uit brandende brandstoffen is in de grootste hoeveelheid en draagt bij aan de opwarming van de aarde?  Wat produceert elektrische energie?
Wat produceert elektrische energie?  Onderzoekers creëren MRI-achtige techniek voor beeldvorming van magnetische golven
Onderzoekers creëren MRI-achtige techniek voor beeldvorming van magnetische golven Touwtrekken rond de zwaartekracht
Touwtrekken rond de zwaartekracht Woordvergelijking voor corrosie van zilver?
Woordvergelijking voor corrosie van zilver?  Welk seizoen zal de zon de eerste opstaan?
Welk seizoen zal de zon de eerste opstaan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


