
Wetenschap
Fysische eigenschappen van stikstofgas:dichtheid, toestanden en industrieel gebruik
TomekD76/iStock/GettyImages
Stikstof is verantwoordelijk voor 78,1% van de atmosfeer van de aarde. Ondanks zijn inertie – zozeer zelfs dat Lavoisier het ‘azote’ noemde, wat ‘zonder leven’ betekent – is het onmisbaar voor het leven en de industrie, en vormt het de ruggengraat van DNA, landbouwmeststoffen en talloze industriële processen.
Kenmerken
Stikstofgas (N₂) is een niet-metaalachtig, kleurloos, geurloos en smaakloos diatomisch molecuul. Met een atoomnummer van 7 en een atoomgewicht van 14,0067, heeft het een dichtheid van 1,251 gL⁻¹ bij 0°C en een soortelijk gewicht van 0,96737, iets lichter dan lucht. Het tripelpunt, waar gas, vloeistof en vaste stof naast elkaar bestaan, vindt plaats bij –210°C (63K) en 12,6 kPa.
Andere staten
Onder het kookpunt van –195,79°C (77K) condenseert stikstof tot vloeibare stikstof, een heldere, geurloze vloeistof die op water lijkt. Verder afkoelen tot het smeltpunt van –210°C (63K) levert een donzige, sneeuwachtige vaste stof op.
Moleculaire binding
In de meeste verbindingen vormt stikstof driewaardige covalente bindingen. Het N₂-molecuul bevat een opmerkelijk sterke drievoudige binding, ondersteund door vijf valentie-elektronen en een elektronegativiteit van 3,04 (Pauling-schaal), wat de chemische stabiliteit ervan ondersteunt.
Gebruik
De overvloed en de chemische inertie van stikstof maken het van onschatbare waarde in de industrie. Het wordt gebruikt in voedselconserverings- en brandbestrijdingssystemen, beschermt zuurstofgevoelige materialen zoals ijzer, staal en elektronica tijdens de productie en dient als belangrijke grondstof voor de ammoniaksynthese via het Haber-Bosch-proces.
Potentieel
In 2001 werd een onderzoek gepubliceerd in Nature meldden dat onderzoekers van het Carnegie Institution of Washington gasvormige stikstof in een vaste toestand hebben omgezet door het tussen twee diamanten aambeelden te comprimeren onder een druk die gelijk is aan 1,7 miljoen atmosfeer. De resulterende vaste stof leek op ijs, maar had toch een diamantachtig kristalrooster. Toen de druk werd opgeheven bij temperaturen onder –173,15°C (100K), bleef de vaste stof stabiel. Bij de faseovergang komt aanzienlijke energie vrij, wat natuurkundige dr. Richard M. Martin ertoe aanzet te speculeren over het potentieel van stikstof als hoogenergetische raketbrandstof.
 Wat is het product van butanol plus thionylchloride?
Wat is het product van butanol plus thionylchloride?  Wat is het verschil tussen een organische verbinding en anorganische verbinding?
Wat is het verschil tussen een organische verbinding en anorganische verbinding?  Maak een lijst van de subatomaire deeltjes en het isotoopsymbool voor broom zo snel mogelijk?
Maak een lijst van de subatomaire deeltjes en het isotoopsymbool voor broom zo snel mogelijk?  Een 3D-beeldvormingstechniek ontgrendelt eigenschappen van perovskietkristallen
Een 3D-beeldvormingstechniek ontgrendelt eigenschappen van perovskietkristallen Een nanostructuur van silica met chemo-enzymatische compartimentering
Een nanostructuur van silica met chemo-enzymatische compartimentering
 Hoe planten omgaan met het koude daglicht en waarom dit van belang is voor toekomstige gewassen
Hoe planten omgaan met het koude daglicht en waarom dit van belang is voor toekomstige gewassen  NASA-instrumenten afbeelding vuurbal boven Beringzee
NASA-instrumenten afbeelding vuurbal boven Beringzee Plankton als klimaatdriver in plaats van de zon?
Plankton als klimaatdriver in plaats van de zon? Welke onderdelen vormen het menselijk been?
Welke onderdelen vormen het menselijk been?
Het menselijke been is een gecompliceerd stuk machines. Het is alleen in staat om zijn werk te doen door de gecompliceerde interactie van verschillende delen. Elk deel van het been bestaat uit zijn eigen
 Klimaatverandering kan van de Arctische toendra een droger landschap maken
Klimaatverandering kan van de Arctische toendra een droger landschap maken
Hoofdlijnen
- Wat is gentherapie?
- Wat zijn de organen van een cel?
- Wat zijn de 4 kenmerken die eukaryotische en prokaryotische cellen delen?
- Een genetische opstand in het vroege leven voorkomen
- Hoe 'moleculaire machines' genactivatie op gang brengen onthuld
- Welke organellen worden alleen gevonden in bacteriën?
- Is een stoel biotische of abiotische factor?
- Mitochondria:structuur en functie - de krachtpatser van de cel
- Welke kenmerken van enzymen maken ze specifiek voor substraat?
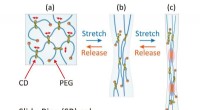
- Biocompatibele hydrogelmaterialen kunnen snel herstellen van mechanische stress
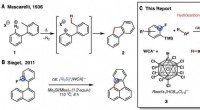
- Functionaliseren van niet-geactiveerde alkanen met behulp van reacties op basis van katalysatoren gemaakt van meer overvloedige materialen
- Groene waterstof:waarom verbeteren bepaalde katalysatoren in werking?

- Het blootleggen van bacteriële celwandgeheimen om antibioticaresistentie te bestrijden

- Onderzoekers optimaliseren materiaalontwerp met behulp van computationele technologieën

 Wat het beste waarom je horizontale strepen ziet in foto's van Jupiter en Saturnus?
Wat het beste waarom je horizontale strepen ziet in foto's van Jupiter en Saturnus?  Gebruiken dolfijnen kogelvissen voor recreatieve doeleinden?
Gebruiken dolfijnen kogelvissen voor recreatieve doeleinden?  Studie beschrijft hoe biomimetische nanomaterialen de schade na een hartaanval kunnen minimaliseren
Studie beschrijft hoe biomimetische nanomaterialen de schade na een hartaanval kunnen minimaliseren  Hoe ontstaan er vlaktes uit de top van een versleten berg?
Hoe ontstaan er vlaktes uit de top van een versleten berg?  Welk stadium wordt beschouwd als de geboorte in een onweersbui?
Welk stadium wordt beschouwd als de geboorte in een onweersbui?  Een golflengte van 2m en een frequentie 5Hz. Hoe snel is het reizen?
Een golflengte van 2m en een frequentie 5Hz. Hoe snel is het reizen?  Hoe een god te zijn:we kunnen ooit virtuele werelden creëren met personages die net zo intelligent zijn als wij
Hoe een god te zijn:we kunnen ooit virtuele werelden creëren met personages die net zo intelligent zijn als wij Wat is het doel van mitose?
Wat is het doel van mitose?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

