
Wetenschap
Hoe het aantal moleculen in een oplossing te berekenen
Door Riti Gupta
Bijgewerkt op 30 augustus 2022
LightFieldStudios/iStock/GettyImages
In het laboratorium werken scheikundigen routinematig met hoeveelheden die astronomisch groot of minuscuul klein zijn. Hoewel een heldere zoutoplossing gemakkelijk te zien is, zijn de individuele moleculen die deze oplossing bevat ver buiten het bereik van het blote oog.
Hoe bepalen we het exacte aantal zoutmoleculen in een bepaald volume? Het antwoord ligt in een fundamentele constante die bekend staat als het getal van Avogadro.
Wat is het getal van Avogadro?
In een zoutoplossing zijn de moleculen onzichtbaar en ontelbaar, vaak groter dan 10 23 in één enkele mol. De scheikunde is afhankelijk van het weten hoeveel deeltjes er aanwezig zijn om reacties te voorspellen, oplossingen voor te bereiden en de nauwkeurigheid van metingen te behouden.
Het concept van de mol overbrugt de kloof tussen deze ondoorgrondelijke hoeveelheden en het dagelijkse laboratoriumwerk. Eén mol van welke stof dan ook bevat precies 6,022 × 10 23 deeltjes:deze waarde staat bekend als het getal van Avogadro.
Denk aan een mol als een dozijn:net zoals een dozijn donuts altijd gelijk is aan twaalf donuts, bevat een mol natriumchloride altijd 6,022 × 10 23 NaCl-moleculen.
De relatie tussen mol en massa wordt uitgedrukt in de molaire massa, het aantal grammen in één mol van een stof. De molaire massa van elk element staat naast het symbool in het periodiek systeem vermeld. De molaire massa van koolstof is bijvoorbeeld 12,01 g/mol, wat betekent dat één mol koolstof 12,01 gram weegt.
Het getal van Avogadro gebruiken om het aantal moleculen te berekenen
Stel dat u 2 mol NaCl heeft. Om uit te vinden hoeveel moleculen dit vertegenwoordigt, vermenigvuldigt u met het getal van Avogadro:
\(\mathrm{2\,mol\,NaCl\Bigl(\frac{6.022\times10^{23}\,\text{moleculen}\,NaCl}{1\,mol}\Bigr)=1.2\times10^{24}\,\text{moleculen}\,NaCl}\)
Dus 2 mol NaCl bevat 1,2 × 10 24 moleculen.
Wat als u 2 gram NaCl krijgt in plaats van moedervlekken? Converteer eerst grammen naar mol met behulp van de molmassa (58,44 g/mol voor NaCl) en pas vervolgens het getal van Avogadro toe:
\(\mathrm{2\,g\,NaCl\Bigl(\frac{1\,mol\,NaCl}{58.44\,g\,NaCl}\Bigr)\Bigl(\frac{6.022\times10 ^{23}\,\text{moleculen}\,NaCl}{1\,mol}\Bigr)=2,1\times10^{22}\,\text{moleculen}\,NaCl}\)
Dus 2 gram NaCl bevat ongeveer 2,1 × 10 22 moleculen.
 Wat zijn de materialen van een luier die vloeistof absorbeert?
Wat zijn de materialen van een luier die vloeistof absorbeert?  Wat is de elementaire samenstelling van een mix van natronkalk en zetmeel?
Wat is de elementaire samenstelling van een mix van natronkalk en zetmeel?  Wetenschappers ontcijferen de structuur, belangrijkste kenmerken van een essentieel immuunsurveillance-eiwit bij mensen
Wetenschappers ontcijferen de structuur, belangrijkste kenmerken van een essentieel immuunsurveillance-eiwit bij mensen Moleculaire tweak verbetert de prestaties van organische zonnecellen
Moleculaire tweak verbetert de prestaties van organische zonnecellen Hoe kan het effect van warmte op een reactie worden bepaald?
Hoe kan het effect van warmte op een reactie worden bepaald?
 Wat zijn twee natuurlijke en kunstmatige bronnen van deeltjes in de atmosfeer?
Wat zijn twee natuurlijke en kunstmatige bronnen van deeltjes in de atmosfeer?  Bewijs gevonden voor Kuroshio-stroomversterking door intensivering van tropische cyclonen
Bewijs gevonden voor Kuroshio-stroomversterking door intensivering van tropische cyclonen Zonnige dagoverstromingen langs de Amerikaanse kust kunnen worden vergroot door de golven van de Atlantische Rossby
Zonnige dagoverstromingen langs de Amerikaanse kust kunnen worden vergroot door de golven van de Atlantische Rossby Kunnen teken eieren bij mensen leggen?
Kunnen teken eieren bij mensen leggen?  Wetenschappers ontcijferen de rol van koolstof en het uiteenvallen van continenten
Wetenschappers ontcijferen de rol van koolstof en het uiteenvallen van continenten
Hoofdlijnen
- Wat is een manier waarop eencellige organismen verschillen van multi-cellige organismen?
- Europese zeebaars vertoont chronische verslechtering na blootstelling aan ruwe olie
- Hoe zijn dieren- en plantencellen vergelijkbaar?
- Kenmerken die worden geërfd, genaamd?
- Een kenmerk van een DNA -molecuul dat geen eiwit is van het molecuul?
- Wat is HemacytoBlast?
- Wat is het verschil tussen symbiotisch en niet-relatie?
- Wat is een soort voedsel dat het eet?
- Wat zijn de belangrijkste delen van de cel?
- Hoe wordt een metaal gevormd?
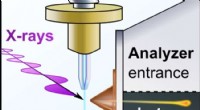
- Ontdekking onthult noodzaak voor ammoniakemissieregelgeving

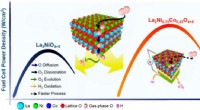
- Nieuw ontdekte ontwerpregels leiden tot betere brandstofcelkatalysator
- Onthul de geheimen van materiaaldegradatie in een lithium-ionbatterij

- Een goedkope, hoogwaardige multinaire intermetallische verbinding als actieve elektrokatalysator voor waterstofproductie

 Welke factoren beïnvloeden het weer?
Welke factoren beïnvloeden het weer?  Hoe is de zon een energiebron voor de aarde?
Hoe is de zon een energiebron voor de aarde?  Het Bohr-model:snel vervangen maar nooit vergeten
Het Bohr-model:snel vervangen maar nooit vergeten  Enorme fouten gevonden in technologie voor gezichtsherkenning:Amerikaans onderzoek
Enorme fouten gevonden in technologie voor gezichtsherkenning:Amerikaans onderzoek Licht is een vorm van energie uitgelegd?
Licht is een vorm van energie uitgelegd?  Dramatische transformatie van woningen in Afrika bezuiden de Sahara voor het eerst onthuld
Dramatische transformatie van woningen in Afrika bezuiden de Sahara voor het eerst onthuld Snelheid definiëren als een snelheid en snelheid definiëren in een gegeven richting?
Snelheid definiëren als een snelheid en snelheid definiëren in een gegeven richting?  Interventie gebaseerd op de wetenschap van lezen en rekenen vergroot het begrip en de vaardigheden om woordproblemen op te lossen
Interventie gebaseerd op de wetenschap van lezen en rekenen vergroot het begrip en de vaardigheden om woordproblemen op te lossen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

