
Wetenschap
Inzicht in diatomische moleculen:structuur, elementen en temperatuureffecten
In de scheikunde is een diatomisch molecuul een verbinding die uit precies twee atomen bestaat. Bij standaardtemperatuur en -druk (STP) zijn de meeste diatomische soorten gassen, en een handvol vaste stoffen verandert bij verhitting in diatomische gassen.
TL;DR
Een diatomisch molecuul bevat twee atomen. De gebruikelijke diatomische elementen zijn H₂, N₂, O₂, F₂, Cl₂, Br₂ en I₂.
Diatomische elementen
Waterstof, stikstof, zuurstof en de halogenen fluor, chloor, broom en jodium vormen bij kamertemperatuur homonucleaire diatomische moleculen. Stikstof is vooral opmerkelijk omdat het door zijn drievoudige binding uitzonderlijk stabiel is.
Edelgassen zoals helium en neon zijn daarentegen monatomisch en vormen onder normale omstandigheden zelden moleculen.
Metalen blijven kristallijne vaste stoffen bij STP en vormen geen homonucleaire diatomische moleculen. Hoewel ze zich kunnen combineren met niet-metalen om ionische verbindingen te produceren (bijvoorbeeld CuCl₂, Fe₂O₃), bevatten deze structuren doorgaans meer dan twee atomen.
Diatomische verbindingen
Heteronucleaire diatomische gassen omvatten koolmonoxide (CO), waterstofchloride (HCl) en stikstofmonoxide (NO). Ondanks dat ze van elkaar verschillen, delen ze dezelfde structuur met twee atomen.
Temperatuurafhankelijke diatomeeën
Hoge temperaturen
Bij verhitting worden bepaalde elementen die bij kamertemperatuur vast zijn, gasvormige diatomische moleculen. Bijvoorbeeld:
- Lithiumdamp vormt dilithium (Li₂).
- Zwaveldamp vormt disulfur (S₂).
- Wolfraamdamp vormt ditungsten (W₂).
- Koolstofdamp kan bestaan als dikoolstof (C₂).
Zelfs ionische vaste stoffen zoals natriumchloride (NaCl) kunnen onder extreme hitte dissociëren in tweeatomige gasmoleculen.
Lage temperaturen
Zuurstof, stikstof en andere diatomische gassen blijven gebonden als moleculen met twee atomen wanneer ze worden afgekoeld tot vloeibare vorm, dankzij intermoleculaire krachten die ze bij elkaar houden onder hun kookpunt.
 Hoe restwarmte-energie op te vangen met verbeterde polymeren
Hoe restwarmte-energie op te vangen met verbeterde polymeren Wat wordt bedoeld met pH?
Wat wordt bedoeld met pH?  Welk symbool in de eerste wet van de thermodynamica vertegenwoordigt een resultaatgas dat zich uitbreidt tegen constante druk?
Welk symbool in de eerste wet van de thermodynamica vertegenwoordigt een resultaatgas dat zich uitbreidt tegen constante druk?  Welke groep is natriumhydroxide in het periodiek systeem?
Welke groep is natriumhydroxide in het periodiek systeem?  Wetenschappers zorgen voor doorbraak vitamine B12
Wetenschappers zorgen voor doorbraak vitamine B12
 Het terugdringen van de uitstoot van steden heeft economische voordelen - en die wegen uiteindelijk op tegen de kosten
Het terugdringen van de uitstoot van steden heeft economische voordelen - en die wegen uiteindelijk op tegen de kosten Kan cocktail-geo-engineering het klimaat redden?
Kan cocktail-geo-engineering het klimaat redden? Aardbevingen kunnen worden verzwakt door grondwater
Aardbevingen kunnen worden verzwakt door grondwater Verzuring van de oceaan kan schelpvorming bevorderen
Verzuring van de oceaan kan schelpvorming bevorderen Portugal riskeert steeds meer dodelijke branden:experts
Portugal riskeert steeds meer dodelijke branden:experts
Hoofdlijnen
- Hoe zijn biotische factoren gerelateerd aan abiotische factoren?
- GTEx Consortium geeft nieuwe inzichten vrij in de manier waarop DNA-verschillen de genexpressie bepalen
- Wat zijn de mechanismen van evolutie?
- Wat dienen als enzymen koolhydraten lipiden lipiden nucleïnezuren eiwitten?
- Er is vlees gemaakt van cellen, en niet van vee. Maar zal het ooit het traditionele vlees vervangen?
- Organismen die het lichaam binnenkomen en je ziek maken, worden ziek?
- Waarom bestaan schimmels?
- Wat is de ontwikkeling van verschillende weefsels?
- Biodiversiteit bij krabben:meer dan alleen soorten tellen
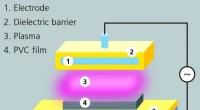
- Plasmabehandeling vermindert de migratie van weekmakers uit bloedzakken
- De eerste in zijn soort chemische oscillator biedt een nieuw niveau van moleculaire controle

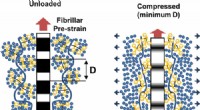
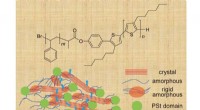
- Collageen in kraakbeenweefsel gedraagt zich als vloeibare kristallen op een smartphonescherm
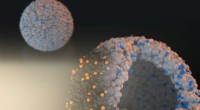
- Heterogene katalysator wordt enzymatisch
- Elektrische verbetering:ingenieurs versnellen elektronen in halfgeleiders
 Goedkoop, schaalbare watersplitsing voedt de toekomstige waterstofeconomie
Goedkoop, schaalbare watersplitsing voedt de toekomstige waterstofeconomie Klei nanobuis-biopolymeer composiet steigers voor tissue engineering
Klei nanobuis-biopolymeer composiet steigers voor tissue engineering Hoe is een kern zoals de echte wereld?
Hoe is een kern zoals de echte wereld?  Nieuwe techniek voor het bestuderen van roesten van staal komt de mijnbouwsector ten goede
Nieuwe techniek voor het bestuderen van roesten van staal komt de mijnbouwsector ten goede Systeem van platte optische lenzen die gemakkelijk in massa kunnen worden geproduceerd en geïntegreerd met beeldsensoren
Systeem van platte optische lenzen die gemakkelijk in massa kunnen worden geproduceerd en geïntegreerd met beeldsensoren Twitter volgt Facebook dat de verkeerde informatie over de volkstelling hardhandig aanpakt
Twitter volgt Facebook dat de verkeerde informatie over de volkstelling hardhandig aanpakt Welke eenheid wordt meestal gebruikt om het volume van een vloeistof te beschrijven?
Welke eenheid wordt meestal gebruikt om het volume van een vloeistof te beschrijven?  Wat is geothermische bron?
Wat is geothermische bron?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

