
Wetenschap
Waarom molmassa belangrijk is in de chemie:een praktische gids
Door Jason Thompson, bijgewerkt op 30 augustus 2022
Bij het inschatten van de hoeveelheid stof die u nodig heeft, kan alleen het gewicht of het volume misleidend zijn. Door variaties in dichtheid kan een zwaar, compact voorwerp veel minder moleculen bevatten dan een lichtgewicht, poreus voorwerp. Chemici overwinnen dit door de mol te gebruiken , een eenheid die deeltjes telt in plaats van massa of ruimte. Eén mol is ongeveer gelijk aan 6,022×10 23 atomen, moleculen of ionen.
Definitie
Molar massa is de massa van één mol van een stof, uitgedrukt in gram per mol (gmol -1 ). Het is de verhouding tussen de massa van een monster en het aantal deeltjes dat het bevat. Als u de molaire massa kent, kunt u met een eenvoudige vermenigvuldiging of deling omrekenen tussen gram en mol.
Experimentele opstelling
Nauwkeurige metingen zijn afhankelijk van de juiste hoeveelheid reactant. Als een protocol bijvoorbeeld 2 mol pure koolstof vereist, berekent u de vereiste massa als volgt:
- Molariteit van koolstof =12,01 gmol -1
- 2mol×12,01gmol -1 =24,02 g
Het gewicht van 24,02 g koolstof zorgt ervoor dat de reactie de exacte stoichiometrische hoeveelheid ontvangt.
Experimentele analyse
Het vergelijken van de volumes die worden ingenomen door gelijke molhoeveelheden van verschillende stoffen onthult inzichten over de moleculaire grootte en pakking. Als 1 mol stof A een groter volume inneemt dan 1 mol stof B, zijn de moleculen van A waarschijnlijk groter of minder efficiënt verpakt.
Massapercentageberekeningen
Molaire massa helpt bij het bepalen van de bijdrage van elk element aan de totale massa van een verbinding. Neem als voorbeeld 28,00 g koolmonoxide (CO):
- Molariteit van koolstof =12,01 gmol -1
- Molar massa zuurstof =16,00 gmol -1
- Totale molmassa van CO =12,01+16,00=28,01gmol -1
- De massafractie van koolstof =(12,01/28,01)×100=42,89%
Koolstof is dus verantwoordelijk voor 42,89% van de massa van CO.
Molaarmassa's voorspellen
Wanneer een nieuwe verbinding wordt gesynthetiseerd, kan de molaire massa ervan worden berekend zonder laboratoriummetingen door de molaire massa's van de samenstellende atomen bij elkaar op te tellen. Deze voorspellende aanpak stroomlijnt de bereiding van reagentia en stoichiometrische berekeningen.
 Hoe zorg je ervoor dat planten op Mars groeien?
Hoe zorg je ervoor dat planten op Mars groeien?  Deeleconomie klinkt zorgzaam, maar laten we het aan de ethische stadstest onderwerpen
Deeleconomie klinkt zorgzaam, maar laten we het aan de ethische stadstest onderwerpen Wat denk je dat er in een ecosysteem zou kunnen gebeuren als het alle soorten planten verloor?
Wat denk je dat er in een ecosysteem zou kunnen gebeuren als het alle soorten planten verloor?  Waarom vallen kruimels op aarde op de grond en niet in de ruimte?
Waarom vallen kruimels op aarde op de grond en niet in de ruimte?  Fracking en aardbevingen - de gevaren in Zuid-Afrika afwegen
Fracking en aardbevingen - de gevaren in Zuid-Afrika afwegen
Hoofdlijnen
- Hoe denkt u dat ziekten de natuurlijke selectie kunnen beïnvloeden?
- Hebben planten of dieren het grootste aantal verschillende cellulaire organellen gemaakt membranen?
- De entic MackeUp van organisme ook de combinatiegenen voor een of meer specifieke eigenschappen?
- Wat is de functie van enzymen in planten?
- Wat voorkomt dat wetenschappers van classyfying plant als protisten als planten?
- Wat zijn de 7 belangrijkste delen van een plantencel?
- Leg uit hoe het ene eiwit verschilt van een ander eiwit?
- Wat zijn de gebreken in klonen?
- Hoe helpen mossen nieuwe biologische gemeenschappen te starten?
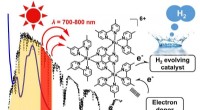
- NIR-gestuurde H2-evolutie uit water:uitbreidend golflengtebereik voor omzetting van zonne-energie
- Waarom katoen de ultieme absorberende stof is

- Nieuw proces kan de energiebehoefte van kunstmest verlagen, op stikstof gebaseerde chemicaliën
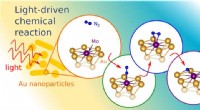
- Anisotrope plasmonen in quasi-metalen 2-D materialen

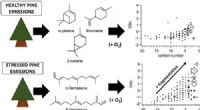
- Bladluis-gestresste dennen vertonen verschillende secundaire organische aerosolvorming
 Wat maakt het zonnestelsel:de dominante elementen
Wat maakt het zonnestelsel:de dominante elementen  Osmotische energiecentrales:benutten van de energie van zoutgradiënten
Osmotische energiecentrales:benutten van de energie van zoutgradiënten  Waar zijn cel -enzymen van gemaakt?
Waar zijn cel -enzymen van gemaakt?  Hoe de zon, de maan en de aarde bewegen:de wetenschap achter dag, nacht en getijden
Hoe de zon, de maan en de aarde bewegen:de wetenschap achter dag, nacht en getijden  Welk gas te gebruiken voor het snijden van plasma?
Welk gas te gebruiken voor het snijden van plasma?  Nieuwe afbeeldingen van asteroïdensonde geven aanwijzingen over planeetvorming (update)
Nieuwe afbeeldingen van asteroïdensonde geven aanwijzingen over planeetvorming (update) Israëlische archeologen onthullen zeldzaam mozaïek uit de Romeinse tijd
Israëlische archeologen onthullen zeldzaam mozaïek uit de Romeinse tijd Wat gebeurt er als de planeten op één lijn liggen?
Wat gebeurt er als de planeten op één lijn liggen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

