
Wetenschap
Berekening van de warmteafgifte bij de zink-zoutzuurreactie
Door Oxana Fox, bijgewerkt op 30 augustus 2022
Zoutzuur (HCl) reageert gemakkelijk met zink (Zn) en produceert zinkchloride (ZnCl₂) en waterstofgas (H₂). Deze reactie is exotherm; de vrijkomende warmte wordt gekwantificeerd door de reactie-enthalpie.
Stap 1 – Schrijf de gebalanceerde vergelijking
Zn + 2 HCl → ZnCl₂ + H₂
Stap 2 – Verzamel standaardformatie-enthalpieën
Standaardenthalpieën (ΔH°ₓf) worden weergegeven in kilojoules per mol (kJmol⁻¹). Voor deze reactie zijn dat:
- Zn (0 kJmol⁻¹)
- HCl (−167,2 kJmol⁻¹)
- ZnCl₂ (−415,1 kJmol⁻¹)
- H₂ (0 kJmol⁻¹)
Stap 3 – Bereken de totale enthalpie van de reactanten
ΣΔH°ₓf (reactanten) = 0 + 2(−167,2) = −334,3 kJmol⁻¹
Stap 4 – Bereken de totale enthalpie van de producten
ΣΔH°ₓf (producten) = −415,1 + 0 = −415,1 kJmol⁻¹
Stap 5 – Bepaal de reactie-enthalpie
ΔH°rxn = ΣΔH°ₓf (producten) − ΣΔH°ₓf (reactanten) = −415,1 − (−334,3) = −80,8 kJmol⁻¹
Het negatieve teken geeft aan dat bij de reactie ongeveer 81 kJ warmte vrijkomt per verbruikte mol zink.
Voor meer gedetailleerde thermodynamische gegevens, zie het NIST Chemistry WebBook .
 Wanneer water het een fysieke verandering of chemische verandering bevriest?
Wanneer water het een fysieke verandering of chemische verandering bevriest?  Waar valt zout in de Mohs Hardness Scale?
Waar valt zout in de Mohs Hardness Scale?  Nieuw elektrodeontwerp kan leiden tot krachtigere batterijen
Nieuw elektrodeontwerp kan leiden tot krachtigere batterijen Hoe maak je lithiumhydride?
Hoe maak je lithiumhydride?  Onderzoekers krijgen controle over de interne structuur van zelf-geassembleerde composietmaterialen
Onderzoekers krijgen controle over de interne structuur van zelf-geassembleerde composietmaterialen
Hoofdlijnen
- Deeltjes surfen op hun eigen golven en laten zien hoe microben en cellen door het menselijk lichaam bewegen
- Hoe planten tomatenplanten zich voort?
- Hoe een bio-bot te bouwen:Onderzoekers delen het ontwerp en de ontwikkeling van biologische machines
- Welk meerlagig epitheel met kubusvormige basale cellen en plat aan het oppervlak zou worden geclassificeerd als?
- Wat is een andere naam voor een gewone microscoop?
- Verre verwante virussen delen zelfassemblagemechanisme
- Wat is het verschil tussen een eencellige en meercellige organisatie?
- Wat zijn analogieën voor chromosomen?
- Wat is wetenschappelijke notatie voor 420?
- Een legering die zijn geheugen behoudt bij hoge temperaturen

- Een betaalbare manier om schone energie op te slaan

- Microanalyse van biologische monsters voor vroege detectie van ziekten
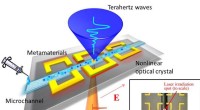
- Moleculen net zo gemakkelijk vastbinden als veters

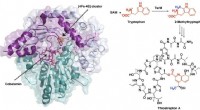
- Synthese van krachtig antibioticum volgt ongebruikelijke chemische route
 Onderzoekers simuleren processen die heersen in vroege magma-oceanen
Onderzoekers simuleren processen die heersen in vroege magma-oceanen Welke beschrijft het beste hoe ons begrip van DNA en erfelijke eigenschappen in de loop van de tijd is veranderd?
Welke beschrijft het beste hoe ons begrip van DNA en erfelijke eigenschappen in de loop van de tijd is veranderd?  Wetenschappers leggen uit waarom sommige origami niet vouwen onder druk
Wetenschappers leggen uit waarom sommige origami niet vouwen onder druk Welke stikstofbasis is aanwezig in RNA maar geen DNA?
Welke stikstofbasis is aanwezig in RNA maar geen DNA?  Wetenschappers werpen licht op organische fotovoltaïsche eigenschappen
Wetenschappers werpen licht op organische fotovoltaïsche eigenschappen Wat zijn de belangrijkste ideeën van de Atomic -theorie van Deltons?
Wat zijn de belangrijkste ideeën van de Atomic -theorie van Deltons?  Gespierde mannen geven de voorkeur aan een ongelijke samenleving
Gespierde mannen geven de voorkeur aan een ongelijke samenleving Wat zijn de twee verschillende soorten energie?
Wat zijn de twee verschillende soorten energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

