
Wetenschap
Berekening van de broomproductie uit broomtrifluoride (BrF₃)
De reactie begrijpen
Broomtrifluoride (BrF₃) is een krachtig oxidatiemiddel en kan met veel stoffen reageren, inclusief zichzelf. Een veel voorkomende reactie is de disproportioneringsreactie waarbij BrF3 reageert en broom (Br₂) en broompentafluoride (BrF₅) vormt:
3 BrF3 → Br₂ + 2 BrF₅
Stoichiometrie en berekening
* De vergelijking in evenwicht brengen: De bovenstaande vergelijking is al in evenwicht. Dit betekent dat 3 mol BrF3 reageert tot 1 mol Br2.
* Molen BrF₃: Je krijgt 0,196 mol BrF₃.
* Mollen Br₂: Met behulp van de stoichiometrische verhouding uit de gebalanceerde vergelijking:
(0,196 mol BrF₃) * (1 mol Br₂ / 3 mol BrF₃) =0,0653 mol Br₂
Daarom zal er bij de volledige reactie van 0,196 mol broomtrifluoride 0,0653 mol broom worden gevormd.
 Is chemische of fysische verandering belangrijker?
Is chemische of fysische verandering belangrijker?  Wat is het punt waarop lucht verzadigd raakt met watermoleculen als gevolg van koeling genoemd?
Wat is het punt waarop lucht verzadigd raakt met watermoleculen als gevolg van koeling genoemd?  Welke 2 stoffen vormen de ruggengraat of zijkanten van het DNA -molecuul?
Welke 2 stoffen vormen de ruggengraat of zijkanten van het DNA -molecuul?  Is steenkool naar vloeistof efficiënter dan benzine?
Is steenkool naar vloeistof efficiënter dan benzine?  Wat zijn de namen van 4 processen die van toestand veranderen als het gaat om gas, vloeibare en vaste stoffen?
Wat zijn de namen van 4 processen die van toestand veranderen als het gaat om gas, vloeibare en vaste stoffen?
 Emissies in savannes verdrievoudigen eerdere schattingen
Emissies in savannes verdrievoudigen eerdere schattingen Vormt Niagara Falls een barrière tegen visbewegingen?
Vormt Niagara Falls een barrière tegen visbewegingen?  Korstmossen:habitats, aanpassingen en symbiotische relaties - een uitgebreide gids
Korstmossen:habitats, aanpassingen en symbiotische relaties - een uitgebreide gids  Er is meer rapportage nodig om de voortgang van de gemeentelijke klimaat- en duurzaamheidsplannen in Ontario aan te tonen, zegt het onderzoek
Er is meer rapportage nodig om de voortgang van de gemeentelijke klimaat- en duurzaamheidsplannen in Ontario aan te tonen, zegt het onderzoek  Beteken minder bomen meer koolstofdioxide?
Beteken minder bomen meer koolstofdioxide?
Hoofdlijnen
- Hoeveel organen heeft een dierencel?
- Komt celafval voort uit activiteiten?
- Uitleggen waarom het proces van mitose en meiose beide zijn?
- Wat is een voorbeeld van Granum?
- Wanneer sporen ontkiemen, welke generatie ontwikkelt zich?
- Welke structuur hebben eukaryoten in hun cel?
- Structuur van tarwe-immuun-eiwit opgelost:belangrijk hulpmiddel in de strijd om voedselzekerheid
- Wat is de naam van een complex individu dat orgaansystemen bestaat?
- Inzicht in purines en pyrimidines:belangrijke nucleïnezuurbasen
- Hybride elektro-biosysteem upcyclet koolstofdioxide tot energierijke verbindingen met lange ketens
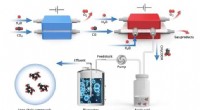
- De weg vrijmaken voor efficiëntere waterstofauto's
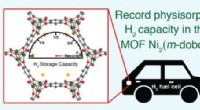
- Groene waterstof:roest als fotoanode en zijn grenzen

- De code van colibactines kraken:onderzoek onderzoekt hoe verbinding DNA beschadigd om het verband met kanker te begrijpen
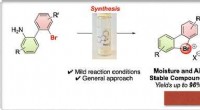
- Cyclische hypervalente brooms werken als aryneprecursoren
 India beoordeelt technisch probleem dat maanmissie afbrak
India beoordeelt technisch probleem dat maanmissie afbrak Een jaar later, EU heeft 145, 000 klachten over gegevenswet
Een jaar later, EU heeft 145, 000 klachten over gegevenswet Waarom is vacuüm de beste thermische isolator?
Waarom is vacuüm de beste thermische isolator?  Ontrafel een verbijsterend explosief proces dat zich in het hele universum voordoet
Ontrafel een verbijsterend explosief proces dat zich in het hele universum voordoet Hoeveel energie kan een getijdenfaciliteit in één jaar produceren?
Hoeveel energie kan een getijdenfaciliteit in één jaar produceren?  Hoe verschillen de rotaties en de revolutie van de aarde?
Hoe verschillen de rotaties en de revolutie van de aarde?  Wat zijn de vier broedprocessen van bodemgenese?
Wat zijn de vier broedprocessen van bodemgenese?  Hoe slaan we extra energie op?
Hoe slaan we extra energie op?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

