
Wetenschap
pH versus pOH:zuurgraad en alkaliteit begrijpen
* pH: Een maat voor de concentratie waterstofionen (H+) in een oplossing. Een lagere pH betekent een hogere concentratie H+-ionen, wat wijst op de zuurgraad.
* pOH: Een maatstaf voor de concentratie hydroxide-ionen (OH-) in een oplossing. Een lagere pOH betekent een hogere concentratie OH-ionen, wat wijst op alkaliteit.
Verband tussen pH en pOH:
* pH + pOH =14 (bij 25 graden Celsius)
Zo kun je bepalen welk ion zich in een hogere concentratie bevindt:
* pH minder dan 7: De oplossing is zuur, wat betekent dat de concentratie H+-ionen groter is dan de concentratie OH-ionen.
* pH groter dan 7: De oplossing is alkalisch (basisch), wat betekent dat de concentratie OH-ionen groter is dan de concentratie H+-ionen.
* pH gelijk aan 7: De oplossing is neutraal, wat betekent dat de concentraties van H+ en OH-ionen gelijk zijn.
Voorbeeld:
* Een oplossing met een pH van 3 heeft een hogere concentratie H+-ionen dan OH-ionen.
* Een oplossing met een pOH van 11 heeft een hogere concentratie OH-ionen dan H+-ionen.
Belangrijke opmerking: De termen "grotere concentratie" en "hogere concentratie" zijn in deze context in essentie uitwisselbaar.
 Plastic microvezels voor het eerst gevonden in ontlasting van wilde dieren van Zuid-Amerikaanse pelsrobben
Plastic microvezels voor het eerst gevonden in ontlasting van wilde dieren van Zuid-Amerikaanse pelsrobben in de eerste, oceaandrone maakt beelden van binnenin orkaan
in de eerste, oceaandrone maakt beelden van binnenin orkaan Informatie over woestijndieren & planten
Informatie over woestijndieren & planten Zal het verlies aan plantendiversiteit de levensondersteunende systemen van de aarde in gevaar brengen?
Zal het verlies aan plantendiversiteit de levensondersteunende systemen van de aarde in gevaar brengen?  Hoe wordt land gebruikt als een fysieke hulpbron?
Hoe wordt land gebruikt als een fysieke hulpbron?
Hoofdlijnen
- Hoe ERF1 de bloei reguleert
- Welk woord heeft de betekenis afgeleid van een levend organisme?
- Hoe zou een organisme waarschijnlijk worden beïnvloed door een DNA -mutatie?
- Welke vier chemische structuren hebben DNA en RNA gemeen?
- Chinese fossielen laten zien dat het menselijke middenoor is geëvolueerd uit de kieuwen van vissen
- Hoe is de kern van spermacellen anders dan in lichaamscel?
- Wat zijn plantenvoortplanting?
- Ecologische soortvorming door seksuele selectie op goede genen:is adaptief?
- Wat zijn voorbeelden van één gram?
- Bij nadere beschouwing blijkt uit magnesium dat zeer kleine monsters veel kneedbaarder zijn dan gedacht

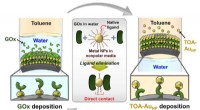
- Elektrodeontwerp maakt de weg vrij voor betere biobrandstofcellen, elektrochemische apparaten
- 3D-geprint apparaat detecteert biomarkers van vroeggeboorte

- Spinzijde inspireert een nieuw materiaal met buitengewone mechanische eigenschappen

- Hoe het massanummer van een element te bepalen

 Statussymbolen in chemische vergelijkingen begrijpen:een uitgebreide gids
Statussymbolen in chemische vergelijkingen begrijpen:een uitgebreide gids  Is de Rigel -ster beweegt naar of weg van de aarde?
Is de Rigel -ster beweegt naar of weg van de aarde?  Nieuwe optische geheugencel bereikt recorddichtheid van gegevensopslag
Nieuwe optische geheugencel bereikt recorddichtheid van gegevensopslag Hoe weet ik of mijn katalysator defect is?
Hoe weet ik of mijn katalysator defect is?  Waarom geleiden moleculaire verbindingen geen elektriciteit?
Waarom geleiden moleculaire verbindingen geen elektriciteit?  Reduceren, hergebruiken, reflycleeren:hoe genetisch gemodificeerde vliegen afval kunnen verminderen en uit de stortplaatsen kunnen houden
Reduceren, hergebruiken, reflycleeren:hoe genetisch gemodificeerde vliegen afval kunnen verminderen en uit de stortplaatsen kunnen houden  Waarom zijn wetenschappers zo geïnteresseerd in genetica?
Waarom zijn wetenschappers zo geïnteresseerd in genetica?  Welke landvorm is niet gebruikelijk in een gebied van Karst -topografie?
Welke landvorm is niet gebruikelijk in een gebied van Karst -topografie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

