
Wetenschap
Zuren begrijpen:eigenschappen, kenmerken en definities
Gemeenschappelijke kenmerken van zuren:
* Smaak: Zuren smaken doorgaans zuur. (Wees voorzichtig, proef nooit chemicaliën!)
* Reactie met basen: Zuren reageren met basen om zouten en water te vormen. Dit staat bekend als neutralisatie.
* Reactie met metalen: Veel zuren reageren met metalen om waterstofgas te produceren.
* Effect op indicatoren: Zuren veranderen de kleur van bepaalde indicatoren, zoals lakmoespapier (waardoor het rood wordt).
* pH: Zuren hebben een pH-waarde lager dan 7.
Definities van zuren:
1. Arrhenius-definitie: Dit is de eenvoudigste en meest bekende definitie. Er wordt gesteld dat een zuur een stof is die waterstofionen (H+) produceert wanneer deze in water wordt opgelost.
* Voorbeeld:HCl (zoutzuur) dissocieert in water en vormt H+ en Cl- ionen.
2. Brønsted-Lowry-definitie: Deze bredere definitie stelt dat een zuur een stof is die een proton (H+) aan een andere stof kan doneren.
* Voorbeeld:Bij de reactie tussen HCl en water doneert HCl een proton aan water, waarbij H3O+ (hydroniumion) en Cl- worden gevormd.
3. Lewis-definitie: Dit is de meest algemene definitie. Er wordt gesteld dat een zuur een stof is die een paar elektronen kan opnemen.
* Voorbeeld:Boriumtrifluoride (BF3) kan een elektronenpaar van ammoniak (NH3) opnemen.
Belangrijkste punten om te onthouden:
* De Arrhenius-definitie is een speciaal geval van de Brønsted-Lowry-definitie.
* De Lewis-definitie is de meest algemene en omvat zowel Brønsted-Lowry- als Arrhenius-zuren.
* De eigenschappen van zuren houden rechtstreeks verband met de aanwezigheid van waterstofionen (H+).
Laat het me weten als je nog vragen hebt over zuren!
 Zonder de Noord-Amerikaanse moesson, Bosbranden in bedwang houden wordt moeilijker
Zonder de Noord-Amerikaanse moesson, Bosbranden in bedwang houden wordt moeilijker Wat behoren wetenschap en kunst tot de hele wereld voordat ze de barrières van nationaliteit verdwijnen?
Wat behoren wetenschap en kunst tot de hele wereld voordat ze de barrières van nationaliteit verdwijnen?  Afvalwaterlek in West-Texas onthuld door satellietradarbeelden en geavanceerde modellering
Afvalwaterlek in West-Texas onthuld door satellietradarbeelden en geavanceerde modellering NASA ziet Irma sterker worden tot orkaan van categorie 5
NASA ziet Irma sterker worden tot orkaan van categorie 5 Wat vormt de aarde de aarde?
Wat vormt de aarde de aarde?
Hoofdlijnen
- Waarom jagen vrouwelijke pinguïns eerst op eten?
- De ploid van een cel in metafase is u haploïde?
- Doodt klimaatverandering Amerikaanse zeesterren?
- Welk orgaan bestaat uit gemodificeerde postganglionische neuronen zonder dendrities of axonen?
- Waarom zijn variabele belangrijk in de wetenschap?
- Wat zijn slechte dingen die nucleus doen?
- De rol van DNA in cellen:blauwdruk van leven en genetische informatie
- Wat is een uiercel?
- Hoe vaccineer je een honingbij? Zes vragen beantwoord over een nieuw instrument om bestuivers te beschermen
- Nieuwe technologie heeft tot doel de levensduur van lithium-metaalbatterijen te verbeteren, veiligheid
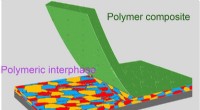
- Een polymere liefdeshormoonsensor voor de vroege detectie van autisme

- Gevoelige nieuwe test detecteert antilichamen tegen SARS-CoV-2 in slechts 10 minuten

- Welke lasser is het beste voor aluminium? TIG, MIG en toorts uitgelegd

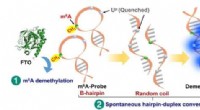
- Nieuwe sonde voor stofwisselingsziekten
 Wat is de definitie van RNA?
Wat is de definitie van RNA?  Onderzoekers onderzoeken hoe de Antarctische ijskappen zullen reageren op de klimaatverandering en de mondiale zeespiegelstijging
Onderzoekers onderzoeken hoe de Antarctische ijskappen zullen reageren op de klimaatverandering en de mondiale zeespiegelstijging  Hoe energie verandert zijn vormen?
Hoe energie verandert zijn vormen?  Wat is het co -enzym van fotosynthese?
Wat is het co -enzym van fotosynthese?  Hoe lang duurt het voordat chloorgas effect heeft?
Hoe lang duurt het voordat chloorgas effect heeft?  Wat is het nut voor fylogenetische bomen?
Wat is het nut voor fylogenetische bomen?  Hoe beïnvloeden planten de landvorm van de aarde?
Hoe beïnvloeden planten de landvorm van de aarde?  Een bacteriecel die plasmide -DNA heeft opgenomen, is?
Een bacteriecel die plasmide -DNA heeft opgenomen, is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

