
Wetenschap
Waterstofbinding:covalente bindingen in H₂-moleculen begrijpen
Dit is waarom:
* Elektronen delen: Elk waterstofatoom heeft één elektron in zijn buitenste schil. Om een stabiele elektronenconfiguratie (zoals helium) te bereiken, delen ze allebei hun elektronen. Hierdoor ontstaat een gedeeld elektronenpaar tussen de twee waterstofatomen.
* Sterke band: Het gedeelde elektronenpaar creëert een sterke aantrekkingskracht tussen de twee positief geladen waterstofkernen en de negatief geladen elektronenwolk. Dit is wat de waterstofatomen bij elkaar houdt om een molecuul te vormen.
* Lagere energie: Bij de vorming van de binding komt energie vrij, wat aangeeft dat het molecuul zich in een lagere energietoestand bevindt dan de twee individuele atomen.
Daarom is het waterstofmolecuul een klassiek voorbeeld van een covalente binding , waarbij twee atomen elektronen delen om stabiliteit te bereiken.
 Het barsten van oliedruppels onder water:hoe vervuiling in het water kan achterblijven na het opruimen van lekkages
Het barsten van oliedruppels onder water:hoe vervuiling in het water kan achterblijven na het opruimen van lekkages  Broombindingen:covalente binding uitgelegd
Broombindingen:covalente binding uitgelegd  Wat is het formulat voor Copper II Chlorate?
Wat is het formulat voor Copper II Chlorate?  Ontdekking voor het groeperen van atomen roept Pasteur . op
Ontdekking voor het groeperen van atomen roept Pasteur . op Wat is het doel van ammoniumchloridepasta in droge cellen?
Wat is het doel van ammoniumchloridepasta in droge cellen?
 De wetlands aan de kust kunnen de stijging van de zeespiegel niet bijhouden, en de infrastructuur zorgt ervoor dat ze nergens heen kunnen
De wetlands aan de kust kunnen de stijging van de zeespiegel niet bijhouden, en de infrastructuur zorgt ervoor dat ze nergens heen kunnen  4D-terugprojectiemethode onthult seismische activiteit die in 2015 in de onderste mantel begon
4D-terugprojectiemethode onthult seismische activiteit die in 2015 in de onderste mantel begon Door welk proces komt water in de atmosfeer van het oppervlak van planten?
Door welk proces komt water in de atmosfeer van het oppervlak van planten?  Kan water of lucht door hout passeren?
Kan water of lucht door hout passeren?  Wat is de betekenis van Hebibore?
Wat is de betekenis van Hebibore?
Hoofdlijnen
- Wat is een meercellige organisim?
- Habitatverlies is de grootste bedreiging voor Australische soorten
- Hoe is het verschil tussen organismen?
- Wat is de inososfeer?
- Welk type weefsel biedt bescherming voor de plant?
- Eiwit-overexpressieprotocol
- Onderzoek naar de genetica van macroalgen werpt licht op hoe zeewier meercellig werd
- Als eiwitten uit aminozuren worden gemaakt, is dat dan een chemische of fysieke verandering?
- Waarom gebruiken wetenschappers modellen van natuurlijke systemen die uw antwoord niet vertellen?
- Genenschaar gebruiken om ziekten op te sporen

- We huwen wanorde met orde:de effecten van geometrische wanorde op vloeistoffen en vaste stoffen in mesoporeuze materialen

- Een nanostructuur van silica met chemo-enzymatische compartimentering

- Onderzoekers maken 's werelds snelste moleculaire shuttle
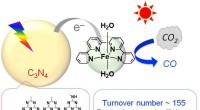
- CO2 verminderen met gemeenschappelijke elementen en zonlicht
 Wetenschappers die waterstof, zuurstof en basisstoffen bestuderen:een gids
Wetenschappers die waterstof, zuurstof en basisstoffen bestuderen:een gids  Wat zijn eencellige micro-organismen die in vijverwater leven?
Wat zijn eencellige micro-organismen die in vijverwater leven?  In welke categorie valt kernenergie?
In welke categorie valt kernenergie?  Wat is bacteriën op de een of andere manier verantwoordelijk voor alle op één behalve een van de processenomgeving?
Wat is bacteriën op de een of andere manier verantwoordelijk voor alle op één behalve een van de processenomgeving?  Wetenschappers beoordelen hoe groot dinosaurussen werkelijk kunnen worden
Wetenschappers beoordelen hoe groot dinosaurussen werkelijk kunnen worden  Hoe noem je een object dat de atmosfeer overleeft en het oppervlak raakt?
Hoe noem je een object dat de atmosfeer overleeft en het oppervlak raakt?  Fluorescerende vloeistof maken
Fluorescerende vloeistof maken Waar leggen reptielen typisch hun eieren?
Waar leggen reptielen typisch hun eieren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

