
Wetenschap
Methylgroepen en extractie:de eigenschappen van oplosmiddelen begrijpen
Hoewel methaan bij kamertemperatuur en druk een gas is, is het geen goed extractieoplosmiddel om verschillende redenen:
1. Lage polariteit: Methaan is extreem apolair vanwege de symmetrische structuur en het ontbreken van polaire bindingen. Dit maakt het slecht in het oplossen van polaire verbindingen .
2. Laag kookpunt: Methaan heeft een zeer laag kookpunt (-161,5 °C), waardoor het bij standaardtemperaturen moeilijk als oplosmiddel te gebruiken is.
3. Veiligheidsproblemen: Methaan is zeer brandbaar en een krachtig broeikasgas.
4. Slechte oplosbaarheid: Methaan heeft een zeer beperkte oplosbaarheid in water en andere gebruikelijke oplosmiddelen.
Samenvattend is methaan een slecht extractieoplosmiddel vanwege zijn niet-polaire aard, laag kookpunt, veiligheidsproblemen en beperkte oplosbaarheid.
Voor effectieve extractie zijn oplosmiddelen met de juiste polariteit en oplosbaarheidseigenschappen nodig . Veel voorkomende oplosmiddelen die bij extractie worden gebruikt, zijn onder meer:
* Hexaan: Een niet-polair oplosmiddel dat wordt gebruikt voor het extraheren van niet-polaire verbindingen zoals vetten en oliën.
* Dichloormethaan: Een oplosmiddel met matige polariteit dat wordt gebruikt voor het extraheren van een verscheidenheid aan verbindingen.
* Ethanol: Een polair oplosmiddel dat wordt gebruikt voor het extraheren van polaire verbindingen zoals suikers en alcoholen.
Houd er rekening mee dat de keuze van het oplosmiddel afhangt van de specifieke verbindingen die worden geëxtraheerd en hun eigenschappen.
 De toxiciteit van banden wordt opnieuw onder de loep genomen na het afsterven van zalm
De toxiciteit van banden wordt opnieuw onder de loep genomen na het afsterven van zalm  Dieren die in de hemellaag van het regenwoud leven
Dieren die in de hemellaag van het regenwoud leven  NASA vindt grote tropische cycloon Marcus sterker
NASA vindt grote tropische cycloon Marcus sterker Twin cyclonen slagman Australië
Twin cyclonen slagman Australië Hoe het SuperNEMO-experiment het mysterie van de oorsprong van materie in het universum zou kunnen helpen oplossen
Hoe het SuperNEMO-experiment het mysterie van de oorsprong van materie in het universum zou kunnen helpen oplossen
Hoofdlijnen
- Wat voor soort virusinfectbacteriën?
- WHON -functies hebben restrictie -enzymen in levende cellen?
- Wat laat bepaalde materialen in en uit de cel passeren?
- Welk type cellen vormen kraakbeen?
- Welke wordt gevonden in zowel RNA als DNA?
- Leg drie kenmerken uit die DNA van RNA onderscheiden?
- Worden sponscellen georganiseerd in weefsels?
- DNA-barcodes:zijn ze altijd nauwkeurig?
- De assemblage van plantendieren en microben die de levende porties vormen die ecosystemen collectief worden genoemd als de?
- Het stimuleren van chemische reacties in vaste toestand
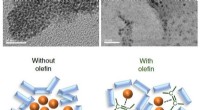
- Het molecuul begrijpen en beheersen dat het universum heeft gemaakt

- Chemici gebruiken de zon om plastic afval te recyclen

- Na het koken, bioversterkte maïs en eieren behouden de voedingsstoffen die nodig zijn om blindheid te voorkomen
- Nieuwe 2D-spectroscopiemethoden

 Welke energiebron voedingsweersystemen?
Welke energiebron voedingsweersystemen?  Welke landen bevinden zich op 70 graden North Latitude?
Welke landen bevinden zich op 70 graden North Latitude?  Lichaamsorgaan dat zoutzuur produceert?
Lichaamsorgaan dat zoutzuur produceert?  Hoe een plant zijn groei reguleert
Hoe een plant zijn groei reguleert  Verbetering van de katalysator die methaan omzet in syngas
Verbetering van de katalysator die methaan omzet in syngas Tatoeage-inkten blijken niet overeen te komen met de ingrediënten vermeld op de fles
Tatoeage-inkten blijken niet overeen te komen met de ingrediënten vermeld op de fles  LAN is de formule -eenheid voor welke ionische verbinding?
LAN is de formule -eenheid voor welke ionische verbinding?  Hoe wordt ijzererts gescheiden van rots?
Hoe wordt ijzererts gescheiden van rots?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

