
Wetenschap
Inzicht in de zuursterkte:sterke versus zwakke zuren uitgelegd
Zuren
* Sterke zuren: Volledig ioniseren (dissociëren) in water, wat betekent dat ze al hun waterstofionen (H+) aan de oplossing doneren.
* Voorbeelden:Zoutzuur (HCl), zwavelzuur (H₂SO₄), salpeterzuur (HNO₃)
* Zwakke zuren: In water ioniseren ze slechts gedeeltelijk, wat betekent dat ze slechts een klein deel van hun waterstofionen doneren. Ze bestaan in evenwicht met hun geconjugeerde base.
* Voorbeelden:Azijnzuur (CH₃COOH), koolzuur (H₂CO₃), citroenzuur (C₆H₈O₇)
Basis
* Sterke basis: Volledig dissociëren in water, waarbij hydroxide-ionen (OH-) vrijkomen in de oplossing.
* Voorbeelden:natriumhydroxide (NaOH), kaliumhydroxide (KOH), calciumhydroxide (Ca(OH)₂)
* Zwakke basen: In water ioniseren ze slechts gedeeltelijk, wat betekent dat ze slechts een klein deel van de beschikbare waterstofionen (H+) accepteren. Ze bestaan in evenwicht met hun geconjugeerde zuur.
* Voorbeelden:Ammoniak (NH₃), methylamine (CH₃NH₂), pyridine (C₅H₅N)
Belangrijke factoren die de kracht bepalen:
* Verbindingssterkte: Sterke zuren hebben zwakke bindingen met hun waterstofatomen, waardoor ze gemakkelijk H+ kunnen doneren. Zwakke zuren hebben sterkere bindingen met hun waterstofatomen.
* Polariteit: Polaire moleculen zijn doorgaans sterkere zuren of basen, omdat de polaire bindingen het gemakkelijker maken om H+-ionen te doneren of te accepteren.
* Grootte van het molecuul: Grotere moleculen met meer elektronen kunnen de negatieve lading die ontstaat wanneer een proton verloren gaat (voor zuren) of de positieve lading die ontstaat wanneer een proton wordt gewonnen (voor basen) beter stabiliseren.
* Elektronenzuigende groepen: Groepen die elektronen wegtrekken van het waterstofatoom maken het gemakkelijker voor het waterstofatoom om te vertrekken (voor zuren), waardoor de zuurgraad toeneemt.
Belangrijkste indicatoren:
* pH: Sterke zuren hebben zeer lage pH-waarden (dichter bij 0), terwijl sterke basen zeer hoge pH-waarden hebben (dichter bij 14). Zwakke zuren en basen hebben pH-waarden dichter bij het neutrale punt van 7.
* Evenwichtsconstante (Ka of Kb): Hoe hoger de Ka (zuurdissociatieconstante) of Kb (basedissociatieconstante), hoe sterker het zuur of de base.
* Geleidbaarheid: Sterke zuren en basen zijn betere geleiders van elektriciteit vanwege hun hoge ionisatie.
Samengevat:
De sterkte van een zuur of base wordt bepaald door zijn vermogen om protonen (H+) in oplossing te doneren of te accepteren. Sterke zuren en basen ioniseren volledig, terwijl zwakke zuren en basen slechts gedeeltelijk ioniseren.
 Plastic voedselverpakkingen kunnen schadelijke chemicaliën bevatten die de hormonen en de stofwisseling beïnvloeden, ontdekken onderzoekers
Plastic voedselverpakkingen kunnen schadelijke chemicaliën bevatten die de hormonen en de stofwisseling beïnvloeden, ontdekken onderzoekers  Waarom vindt convectie plaats in een vast materiaal?
Waarom vindt convectie plaats in een vast materiaal?  Fotokatalytische niet-oxidatieve koppeling van methaan aan ethyleen via met koolstof gedoteerde ZnO/Au-katalysatoren
Fotokatalytische niet-oxidatieve koppeling van methaan aan ethyleen via met koolstof gedoteerde ZnO/Au-katalysatoren  Wetenschappers gebruiken hogedruk-NMR-spectroscopie om de structuur van dynamische eiwitten te bestuderen
Wetenschappers gebruiken hogedruk-NMR-spectroscopie om de structuur van dynamische eiwitten te bestuderen  Hoe herkent u exotherme en endothermische reacties?
Hoe herkent u exotherme en endothermische reacties?
 De Antarctica-factor:modelonzekerheden onthullen aanstaand risico op zeeniveau
De Antarctica-factor:modelonzekerheden onthullen aanstaand risico op zeeniveau Waarom is het verhaal van de wetenschapscreatie belangrijk?
Waarom is het verhaal van de wetenschapscreatie belangrijk?  Nieuwe studies vergroten het vertrouwen in NASA's meting van de temperatuur op aarde
Nieuwe studies vergroten het vertrouwen in NASA's meting van de temperatuur op aarde Satellietvolging laat zien hoe schepen de wolken en het klimaat beïnvloeden
Satellietvolging laat zien hoe schepen de wolken en het klimaat beïnvloeden Soorten wolken voor kinderen
Soorten wolken voor kinderen
Hoofdlijnen
- Nieuwe studie werpt licht op hoe de vroegste vormen van leven op aarde zijn geëvolueerd
- Hoe dragen mensen bij aan zaadverspreiding?
- Wat voor soort mutatie heeft waarschijnlijk het minste effect op een organisme?
- Het simuleren van seks met walvisachtigen met kadaverdelen biedt inzicht in mariene copulatie
- Basiscelfuncties
- Welke cel wordt mitochondrion gevonden in dier- of plantencel?
- Wat veranderen organismen gedurende lange tijd in lange tijd?
- Hoe groeit een organisme?
- Onderzoekers laten zien hoe deep learning het onderzoek naar neurale degeneratie kan bevorderen
- Stoere liefde:intense schittering helpt next-gen zonnetechnologie door lastige fase

- Surface-enhanced Raman-spectroscopiemethode realiseert kwantitatieve detectie van geneesmiddelen tegen kanker in serum
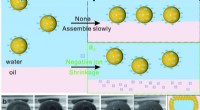
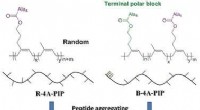
- Biomimetische strategie leidt tot sterke, recyclebaar rubber
- Waarom toekomstige huizen gemaakt kunnen worden van levende schimmel

- Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn
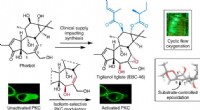
 29 Amerikaanse staten en steden klagen Trump aan wegens klimaatbescherming
29 Amerikaanse staten en steden klagen Trump aan wegens klimaatbescherming Soorten Pijlstaartrogvissen
Soorten Pijlstaartrogvissen Wat kunt u gebruiken om de dichtheid van een mysterieuze vloeistof te evalueren?
Wat kunt u gebruiken om de dichtheid van een mysterieuze vloeistof te evalueren?  Waar zijn drie abiotische factoren waar het aantal en soorten organismen in een ecosysteem van afhangt?
Waar zijn drie abiotische factoren waar het aantal en soorten organismen in een ecosysteem van afhangt?  Welk land bevindt zich 10 graden North en 61 West?
Welk land bevindt zich 10 graden North en 61 West?  Hoe heeft de wetenschap ons geholpen op het gebied van de landbouw?
Hoe heeft de wetenschap ons geholpen op het gebied van de landbouw?  Glycerine maken uit plantaardige olie
Glycerine maken uit plantaardige olie  Wat is de complementaire basispaarregel?
Wat is de complementaire basispaarregel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

