
Wetenschap
Koolstof-elektronegativiteit:hoe de hechting van zuurstof deze vergroot
* Elektronegativiteit: Elektronegativiteit is het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding. Zuurstof is zeer elektronegatief, wat betekent dat het een sterke aantrekkingskracht op elektronen heeft.
* Polaire covalente binding: Wanneer zuurstof zich met koolstof bindt, vormen ze een polaire covalente binding. Dit betekent dat de elektronen in de binding niet gelijk worden verdeeld. Het meer elektronegatieve zuurstofatoom trekt de elektronen dichter naar zichzelf toe, waardoor een gedeeltelijke negatieve lading (δ-) op de zuurstof en een gedeeltelijke positieve lading (δ+) op de koolstof ontstaat.
* Effect op koolstof: Deze gedeeltelijke positieve lading op de koolstof maakt deze gevoeliger voor aanvallen door nucleofielen (elektronenrijke soorten) bij chemische reacties.
Samengevat: De aanwezigheid van een zuurstofatoom gehecht aan een koolstof maakt de koolstof elektronegatiever vanwege de polaire aard van de binding. Dit heeft gevolgen voor de reactiviteit en eigenschappen van het molecuul.
 Microfluïdische chip voor analyse van afzonderlijke cellen
Microfluïdische chip voor analyse van afzonderlijke cellen IJzer veilig oplossen met zoutzuur:een gedetailleerde, stapsgewijze handleiding
IJzer veilig oplossen met zoutzuur:een gedetailleerde, stapsgewijze handleiding  Organokatalysator die radicale reacties regelt voor complexe en omvangrijke synthese van verbindingen
Organokatalysator die radicale reacties regelt voor complexe en omvangrijke synthese van verbindingen Hoeveel atomen zijn er in C16H12O6?
Hoeveel atomen zijn er in C16H12O6?  Een atoom met 1 proton en neutron?
Een atoom met 1 proton en neutron?
 De Indonesische Merapi-vulkaan spuwt hete wolken, 500 evacueren
De Indonesische Merapi-vulkaan spuwt hete wolken, 500 evacueren In Mozambique, een gezamenlijke strijd tegen klimaatverandering en bosverlies
In Mozambique, een gezamenlijke strijd tegen klimaatverandering en bosverlies Ons fysieke begrip van klimaatprocessen verbeteren met behulp van verbeterde klimaatmodellen
Ons fysieke begrip van klimaatprocessen verbeteren met behulp van verbeterde klimaatmodellen De belangrijkste takken van wetenschap geven?
De belangrijkste takken van wetenschap geven?  Hoe helpt de milieuwetenschap ons de natuurlijke wereld te begrijpen?
Hoe helpt de milieuwetenschap ons de natuurlijke wereld te begrijpen?
Hoofdlijnen
- Welke menselijke cel gebruikt fagocytose als een verdedigingsmechanisme?
- Biologische evolutie begrijpen:een uitgebreide gids
- Wat doet de kern in een plantencel?
- Wat regelt de levensprocessen van een cel?
- Wat zijn lange draadachtige structuren die uit de prokaryotische cellen van het oppervlak steken en wat worden gebruikt voor voortbeweging?
- Wat is een analogie voor het metabolisme?
- Wat zijn de stadia van cytokinese?
- Nerveus weefsel bestaat uit cellen die worden genoemd?
- Wat zijn de factoren die ervoor zorgen dat de evolutie zich voordoet?
- Onaangename geuren uit het airconditioningsysteem van uw auto identificeren en oplossen
- Gefuseerde beeldvorming onthult zesde-eeuws schrift verborgen in boekbinden

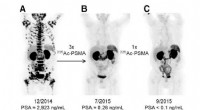
- Hoe wetenschappers een nieuwe manier ontdekten om actinium-225 te produceren, een zeldzame medische radio-isotoop
- Sensor kan bedorven melk detecteren voor opening

- Onderzoekers lossen 100 jaar oude metallurgiepuzzel op

 Hebben rode sterren hogere oppervlaktetemperaturen dan blauwe sterren?
Hebben rode sterren hogere oppervlaktetemperaturen dan blauwe sterren?  Welke organel in de kern maakt ribosomen?
Welke organel in de kern maakt ribosomen?  Welke moleculen voor energietrager produceren door glycolyse?
Welke moleculen voor energietrager produceren door glycolyse?  Planet met snelste baansnelheid in uw zonnestelsel?
Planet met snelste baansnelheid in uw zonnestelsel?  Grafeenoxidepapier verandert met spanning
Grafeenoxidepapier verandert met spanning Verloren of uitgestorven? Uit onderzoek blijkt dat het bestaan van meer dan 500 diersoorten onzeker blijft
Verloren of uitgestorven? Uit onderzoek blijkt dat het bestaan van meer dan 500 diersoorten onzeker blijft  Ons toekomstige klimaat hangt gedeeltelijk af van bodemmicroben, maar hoe worden zij door veranderingen beïnvloed?
Ons toekomstige klimaat hangt gedeeltelijk af van bodemmicroben, maar hoe worden zij door veranderingen beïnvloed?  Hoe fotonicamasten zullen werken
Hoe fotonicamasten zullen werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

