
Wetenschap
Fluor versus broom:vergelijking en uitleg van elektronenaffiniteit
* Kleiner formaat: Fluor is kleiner dan broom. Dit betekent dat het buitenste elektron in fluor zich dichter bij de kern bevindt en een sterkere aantrekkingskracht ervaart.
* Hogere effectieve nucleaire lading: Fluor heeft een hogere effectieve nucleaire lading (de positieve lading die door het buitenste elektron wordt gevoeld) dan broom. Dit komt door de kleinere omvang en het toenemende aantal protonen in de kern naarmate je verder langs de halogeengroep beweegt.
Elektronenaffiniteit is de verandering in energie wanneer een elektron wordt toegevoegd aan een neutraal atoom in gasvormige toestand. Een meer negatieve elektronenaffiniteit duidt op een grotere neiging om een elektron te verwerven.
Daarom resulteren de kleinere omvang van fluor en de hogere effectieve nucleaire lading in een meer negatieve elektronenaffiniteit vergeleken met broom.
Hoofdlijnen
- Kanker op een Paleodieet? Vraag het aan iemand die 1,7 miljoen jaar geleden leefde
- Wat is een type eiwit- of RNA -molecuul dat metabole reacties bij planten en dieren versnelt zonder permanent te worden vernietigd?
- Cellulaire processen zijn over het algemeen beperkt tot welke pH -niveaus?
- Hoe helpen enzymen het organisme efficiënt gebruik te maken van hun energie?
- Welke klier reguleert direct de productie van hormonen in andere klieren?
- Snavels laten zien waarom 'zuster'-soorten niet samenleven
- De functie van veel eiwitten blijft onduidelijk
- Jesse keek naar een cel via microscoop en zag mitochondria membranen wat zou kunnen zeggen over de cel?
- Het cytoplasma van een cel is?
- Een sorteertechnologie die cellen isoleert met een hoge zuiverheid en levensvatbaarheid

- Een nieuwe betaalbare en gebruiksvriendelijke technologie voor de diagnose van droge ogen

- Gecombineerde röntgen- en fluorescentiemicroscoop onthult onzichtbare moleculaire details
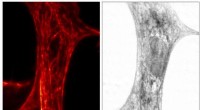
- GLUT5 fluorescerende sonde vingerafdrukken kankercellen
- Synthetisch kanaal met een sterke voorkeur voor kaliumionen biedt snel transport door kunstmembraan

 Hoe kun je zonne -energie veranderen in elektriciteit?
Hoe kun je zonne -energie veranderen in elektriciteit?  Wat is 101.4 Fahrenheit?
Wat is 101.4 Fahrenheit?  Rapportkaarten laten een aanhoudende stijging van de zeespiegel zien aan de oost- en Golfkust
Rapportkaarten laten een aanhoudende stijging van de zeespiegel zien aan de oost- en Golfkust  privacy, eens verborgen onderwerp, krijgt aandacht op CES tech show
privacy, eens verborgen onderwerp, krijgt aandacht op CES tech show Verschillende soorten rupsen
Verschillende soorten rupsen  Afbeelding:Hubble vangt een subtiele zwerm
Afbeelding:Hubble vangt een subtiele zwerm Wat is speciaal aan de maan Europa?
Wat is speciaal aan de maan Europa?  Wat betekent hybride in de wetenschap?
Wat betekent hybride in de wetenschap?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


