
Wetenschap
Zink- en zwavelzuurreactie:het chemische proces begrijpen
De reactie
Zink (Zn) reageert met verdund zwavelzuur (H₂SO₄) en produceert zinksulfaat (ZnSO₄) en waterstofgas (H₂). Dit is een enkele verplaatsingsreactie.
Chemische vergelijking:
Zn(s) + H₂SO₄(aq) → ZnSO₄(aq) + H₂(g)
Uitleg:
1. De reactiviteit van zink: Zink is reactiever dan waterstof. Dit betekent dat zink waterstof uit zijn verbinding, zwavelzuur, kan verdringen.
2. De reactie: Wanneer zink in contact komt met verdund zwavelzuur, gebeurt het volgende:
- De zinkatomen verliezen elektronen (oxidatie) en worden zinkionen (Zn²⁺).
- Waterstofionen (H⁺) uit het zuur winnen elektronen (reductie) en worden waterstofgas (H₂).
3. Vorming van zinksulfaat: De zinkionen (Zn²⁺) combineren met sulfaationen (SO₄²⁻) uit het zuur en vormen zinksulfaat (ZnSO₄), dat oplost in de oplossing.
4. Evolutie van waterstofgas: Het geproduceerde waterstofgas wordt gezien als bellen die naar het oppervlak van de oplossing stijgen.
Opmerkingen:
* Bubbelen: Je zult krachtig borrelen waarnemen terwijl waterstofgas vrijkomt.
* Kleurverandering: De oplossing kan enigszins troebel worden naarmate zinksulfaat oplost.
* Warmtegeneratie: De reactie is exotherm, wat betekent dat er warmte vrijkomt en dat u mogelijk een lichte temperatuurstijging in de oplossing opmerkt.
Belangrijke opmerking: Het bemoste zink helpt het oppervlak van het zink dat in contact komt met het zuur te vergroten, wat de reactiesnelheid versnelt.
Laat het me weten als je nog vragen hebt!
Hoofdlijnen
- Onderzoekers gebruiken genoomanalyse om te begrijpen hoe koningspinguïns op de Crozet-eilanden kwamen broeden
- Beschrijf de functies van twee typen celmembraaneiwitten?
- DNA:de bouwsteen van genen - structuur en componenten
- Welk chromosoom beïnvloedt de ziekte van Tay-Sachs?
- Welke basisstructuur vormt alle levende organismen en maakt ze anders dan niet-dingen?
- T-cellen gebruiken geweld om kankercellen te vernietigen
- Wat stelt de moderne evolutietheorie dat een basis voor variatie binnen soorten wordt verstrekt?
- Wanneer zou een soort verwachten het logistieke groeipatroon te zien doorlopen?
- Wat vormt een groep cellen hetzelfde type?
- Schelpen en grapefruits inspireren het eerste vervaardigde niet-snijbare materiaal

- Fluorescentiepatronen helpen bij medische diagnostiek

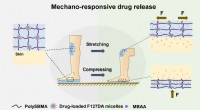
- Mechano-responsieve hydrogel ontwikkeld voor wondgenezing
- Onderzoekers ontdekken een spanning die afhangt van de golflengte van invallend licht

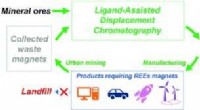
- Technologieën om te extraheren, het zuiveren van kritische zeldzame aardmetalen kan een game changer zijn
 Waarom houden dingen een constante snelheid op een oppervlak van de aarde?
Waarom houden dingen een constante snelheid op een oppervlak van de aarde?  Hoe lang duurt een gemiddelde zonnemaand een twaalfde van een jaar?
Hoe lang duurt een gemiddelde zonnemaand een twaalfde van een jaar?  Wanneer nanoplastics niet zijn wat ze lijken:vrijkomen van oligomeren uit polyestertextiel
Wanneer nanoplastics niet zijn wat ze lijken:vrijkomen van oligomeren uit polyestertextiel  Welke horizon heeft de meeste organische materie in de bodem?
Welke horizon heeft de meeste organische materie in de bodem?  Hoe is Earths Core blijkbaar vergelijkbaar met sommige ijzeren meteorieten?
Hoe is Earths Core blijkbaar vergelijkbaar met sommige ijzeren meteorieten?  Wat zou de beginsnelheid van een raket moeten zijn als deze op 1000 km afstand moet worden geraakt?
Wat zou de beginsnelheid van een raket moeten zijn als deze op 1000 km afstand moet worden geraakt?  Welke planeet heeft vulkaan en berg in het zonnestelsel?
Welke planeet heeft vulkaan en berg in het zonnestelsel?  Wetenschappers bestuderen de organisatie van het leven op planetaire schaal
Wetenschappers bestuderen de organisatie van het leven op planetaire schaal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


