
Wetenschap
Chemische bindingen en energie-uitwisseling:breken en vormen
Energie-input (obligaties verbreken):
* Endotherme reacties: Reacties die energie uit hun omgeving absorberen.
* Het verbreken van obligaties: Wanneer energie in een systeem wordt ingevoerd, kan deze worden gebruikt om de krachten te overwinnen die atomen in een molecuul bij elkaar houden. Deze energie-input verzwakt de verbindingen, waardoor ze uiteindelijk breken.
* Voorbeelden:
* Smeltend ijs:Energie-input verbreekt de waterstofbruggen die watermoleculen in vaste toestand bij elkaar houden.
* Fotosynthese:Zonlicht levert de energie om kooldioxide- en watermoleculen af te breken, waardoor planten suikers kunnen aanmaken.
Energieopbrengst (bindingen vormen):
* Exotherme reacties: Reacties die energie vrijgeven aan hun omgeving.
* Bondvorming: Wanneer er nieuwe bindingen tussen atomen ontstaan, komt er energie vrij. Dit komt omdat de atomen stabieler worden door elektronen te delen, waardoor de overtollige energie vrijkomt als warmte of licht.
* Voorbeelden:
* Hout verbranden:Bij het verbreken van verbindingen in het hout komt energie vrij, die wordt afgegeven in de vorm van warmte en licht.
* Verbranding:Bij het verbranden van brandstoffen zoals benzine worden bestaande bindingen verbroken en nieuwe bindingen in de producten gevormd, waarbij energie vrijkomt in de vorm van warmte en licht.
Belangrijkste punten:
* Er wordt energie bespaard: De totale energie in een systeem blijft constant. Energie wordt niet gecreëerd of vernietigd, maar alleen overgedragen of getransformeerd.
* Verbindingssterkte: Verschillende bindingen hebben verschillende sterke punten. Sterkere bindingen vereisen meer energie om te breken, en bij de vorming ervan komt meer energie vrij.
* Activeringsenergie: Zelfs exotherme reacties vereisen een initiële input van energie (activeringsenergie) om het proces van het verbreken van de binding op gang te brengen.
In wezen is het verbreken en vormen van chemische bindingen van fundamenteel belang voor de energie-uitwisseling bij chemische reacties. Er wordt energie geabsorbeerd om verbindingen te verbreken, en energie komt vrij wanneer verbindingen worden gevormd.
 Hoeveel koolstofatomen zijn aanwezig in een molecuul tetrluoride?
Hoeveel koolstofatomen zijn aanwezig in een molecuul tetrluoride?  Onderzoekers zorgen ervoor dat neurale netwerken met succes DNA-schade door UV-straling detecteren
Onderzoekers zorgen ervoor dat neurale netwerken met succes DNA-schade door UV-straling detecteren Wat gebeurt er wanneer elektriciteit wordt doorgegeven door waterige oplossing van natriumchloride?
Wat gebeurt er wanneer elektriciteit wordt doorgegeven door waterige oplossing van natriumchloride?  Uit welke klasse (Es) van elementen is de volgende verbinding met stikstofdioxide gemaakt?
Uit welke klasse (Es) van elementen is de volgende verbinding met stikstofdioxide gemaakt?  Hoeveel formule-eenheden zitten er in 22,4 g SnO2?
Hoeveel formule-eenheden zitten er in 22,4 g SnO2?
Hoofdlijnen
- Stamcelplatform werpt nieuw licht op het begin van menselijke ontwikkeling
- Waarom zijn alle levende organismen gegroepeerd in classificatiesystemen?
- Hoe wordt het voedsel verteerd geabsorbeerd en naar de cellen getransporteerd?
- Als een lichaamsorganen aanwezig zijn, hoe heet de zich ontwikkelende baby?
- Studie onderzoekt conflict tussen boeren en roofdieren
- Nauwkeurig bijhouden hoe plastic biologisch afbreekt
- Welke aro twee voorstanders van meercellig zijn?
- Onderzoekers laten zien hoe het ontwerp van gebouwen de bacteriën binnenshuis beïnvloedt
- Een universeel raamwerk voor ruimtelijke biologie
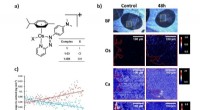
- X-ray fluorescentie mapping om tumorpenetratie te meten door een nieuw middel tegen kanker
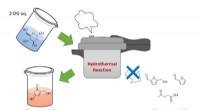
- Ontdekking van elektrokatalysatoren versnellen

- Bacteriën produceren goud door giftige metalen te verteren

- Dubbelwerkende katalysator genereert waterstofbrandstof terwijl afvalwater wordt opgeruimd

- Onderzoekers optimaliseren methoden om bruikbare verbindingen uit biomassa te produceren
 Glucose plus fructose vormen een disacharide genaamd?
Glucose plus fructose vormen een disacharide genaamd?  Hoe bouw je een Covered Wagon Model voor Kinderen
Hoe bouw je een Covered Wagon Model voor Kinderen  Wat is de oorsprong van wolfraam?
Wat is de oorsprong van wolfraam?  BMW beboet voor softwarefout diesel
BMW beboet voor softwarefout diesel Welke materialen beweegt de wind?
Welke materialen beweegt de wind?  Wat is de energiedrager die de meeste soorten cellulair werk in levende cellen voedt?
Wat is de energiedrager die de meeste soorten cellulair werk in levende cellen voedt?  Geladen grafeen geeft DNA een podium om moleculaire gymnastiek uit te voeren
Geladen grafeen geeft DNA een podium om moleculaire gymnastiek uit te voeren Hoe verschilt de rol van energie in fotosynthese en cellulaire ademhaling?
Hoe verschilt de rol van energie in fotosynthese en cellulaire ademhaling?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

