
Wetenschap
Waarom NaCl kookt bij een veel hogere temperatuur dan C4H10 - uitgelegd
* Ionische versus covalente binding: NaCl is een ionische verbinding, wat betekent dat het een kristalroosterstructuur vormt die bij elkaar wordt gehouden door sterke elektrostatische krachten tussen positief geladen natriumionen (Na⁺) en negatief geladen chloride-ionen (Cl⁻). C₄H₁₀ (butaan) is een covalente verbinding, waarbij moleculen bij elkaar worden gehouden door relatief zwakke Van der Waals-krachten.
* Kracht van intermoleculaire krachten: De elektrostatische krachten in ionische verbindingen zijn aanzienlijk sterker dan de Van der Waals-krachten in covalente verbindingen. Dit verschil in de sterkte van de intermoleculaire krachten is de belangrijkste reden voor het enorme kookpuntverschil.
Zo wordt het vertaald naar kookpunt:
* NaCl: Om de sterke ionische bindingen in NaCl te verbreken en het te laten koken, moet je een enorme hoeveelheid energie leveren, wat resulteert in een zeer hoog kookpunt (meer dan 1400°C).
* C₄H₁₀: De zwakke Van der Waals-krachten in butaan kunnen gemakkelijk met relatief weinig energie worden overwonnen, wat leidt tot een veel lager kookpunt (-0,5°C).
Samengevat:
* NaCl: Sterke ionische bindingen =hoge smelt- en kookpunten
* C₄H₁₀: Zwakke Van der Waals-krachten =lage smelt- en kookpunten
 de relatie tussen fundamentele en afgeleide grootheden?
de relatie tussen fundamentele en afgeleide grootheden?  Hoeveel atomen zitten er in 55 mg koolstof?
Hoeveel atomen zitten er in 55 mg koolstof?  Welke van de volgende typen elektromagnetische straling veroorzaakt een bepaalde substantie tot bloem?
Welke van de volgende typen elektromagnetische straling veroorzaakt een bepaalde substantie tot bloem?  Wat is het nummer dat links van het chemische symbool of de formule wordt geschreven?
Wat is het nummer dat links van het chemische symbool of de formule wordt geschreven?  Het suikermetabolisme is verrassend conventioneel bij kanker
Het suikermetabolisme is verrassend conventioneel bij kanker
 Hoe heeft de uitvinding van de microscoop invloed op wetenschappers die levende wezens begrepen?
Hoe heeft de uitvinding van de microscoop invloed op wetenschappers die levende wezens begrepen?  Niet voor altijd:grootste roze diamantmijn ter wereld gaat dicht
Niet voor altijd:grootste roze diamantmijn ter wereld gaat dicht Het geheim van het weerstaan van klimaatverandering ligt aan onze voeten
Het geheim van het weerstaan van klimaatverandering ligt aan onze voeten Soorten die getroffen worden door de klimaatverandering:verschuiven of niet?
Soorten die getroffen worden door de klimaatverandering:verschuiven of niet?  Voordelen en nadelen van woestijnen
Voordelen en nadelen van woestijnen
Hoofdlijnen
- Opmerkelijke Biologen:Pioniers in Evolutionary Science &Beyond
- Een vasculaire plant die zich voortplant met sporen is een varen?
- Waarom deden wetenschappers zo lang om te concluderen dat alle levende dingen van cellen zijn gemaakt, zelfs met de hulp van een microscoop?
- Wat zijn enkele redenen waarom apen gerelateerd aan de wetenschap?
- Waarom hebben planten meiose nodig?
- Wanneer is de endosymbiotische theorie gebeurd?
- Wat is de celstructuur die DNA bevat en de functies van de Calls beheert?
- Wat doet het als je lichaam slechte bacteriën aantrekt?
- Cellulaire ademhaling in ontkiemende zaden
- Atomen versus ionen:belangrijkste verschillen in samenstelling, lading en binding

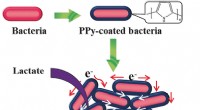
- Geleidende schaal voor bacteriën
- Door goedkope en veilige zwart-witte materialen te combineren, ontstaan kleurrijke pigmenten

- Review benadrukt de kracht van eenvoudige fysieke modellen voor complexe eiwitmachines

- Wetenschappers vinden sneller uit, goedkopere strategie voor het ontwerpen van infrarood-emitterende materialen

 Wat gebeurt er als er niet genoeg wrijving is?
Wat gebeurt er als er niet genoeg wrijving is?  Hoeveel potentieel en kinetische energie gebruikt een gemiddeld persoon een dag?
Hoeveel potentieel en kinetische energie gebruikt een gemiddeld persoon een dag?  Waarom absorbeert de dierlijke cel zonder zuurstof geen natrium?
Waarom absorbeert de dierlijke cel zonder zuurstof geen natrium?  Onderzoekers beschrijven spin-bosonsystemen om kwantumapparaten te configureren
Onderzoekers beschrijven spin-bosonsystemen om kwantumapparaten te configureren  Waarom is de uitwisselingssnelheid van ionen veel lager wanneer de capaciteit van de hars bijna is bereikt?
Waarom is de uitwisselingssnelheid van ionen veel lager wanneer de capaciteit van de hars bijna is bereikt?  Wat is de grootste ster of universum van één Galaxy Solar System?
Wat is de grootste ster of universum van één Galaxy Solar System?  Gekweekte stamcellen reconstrueren sensorische zenuw- en weefselstructuur in de neus
Gekweekte stamcellen reconstrueren sensorische zenuw- en weefselstructuur in de neus Kan housemuziek de energiecrisis oplossen?
Kan housemuziek de energiecrisis oplossen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

