
Wetenschap
Amfotere HSO₄⁻:inzicht in het zuur-base-gedrag ervan
HSO₄⁻ kan zowel als base als als zuur fungeren, omdat het een amfiprotische soort is . Dit betekent dat het een proton kan doneren (werkt als een zuur) of een proton kan accepteren (werkt als een base).
Hier is een overzicht:
Als zuur:
* HSO₄⁻ kan een proton (H⁺) doneren om SO₄²⁻ (sulfaation) te vormen:
HSO₄⁻ ⇌ H⁺ + SO₄²⁻
Als basis:
* HSO₄⁻ kan een proton (H⁺) accepteren om H₂SO₄ (zwavelzuur) te vormen:
HSO₄⁻ + H⁺ ⇌ H₂SO₄
Dit dubbele gedrag is te wijten aan de aanwezigheid van het waterstofatoom gehecht aan het zwavelatoom in HSO₄⁻. Deze waterstof kan vrijkomen als proton (zuur gedrag) of kan worden toegevoegd om een andere binding te vormen (basisch gedrag).
Samengevat:
HSO₄⁻ is een amfiprotische soort, wat betekent dat het zowel als zuur als als base kan werken, afhankelijk van de reactieomgeving.
Hoofdlijnen
- Met welk deel van een cel kan stoffen erdoorheen gaan?
- Zijn alle cellen hetzelfde, zo niet op welke manieren zijn ze anders?
- Hoe menselijke transportgewoonten het gedrag van kleine mijten helpen verklaren
- Biofysici meten voor het eerst wat er gebeurt als rode bloedcellen ‘kronkelen’
- Wat is het proces van het maken van mRNA van code in DNA opgeroepen?
- Wat zijn drie dingen die een wetenschappelijke naam kan vertellen over het organisme?
- Wat is een virale infectie waardoor de gastheercel barst en sterft om het nieuw gesynthetiseerd virus vrij te geven?
- Wat is de twee classificatie van planten?
- Wat is het koninkrijk van rode algen?
- Ontleden van colloïdale glazen met laser als lancet
- Onderzoek levert potentiële bioblendstock op voor dieselbrandstof

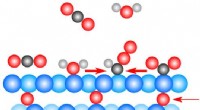
- Onderzoekers vinden een verrassing net onder het oppervlak in een koolstofdioxide-experiment
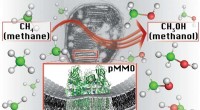
- Methaanverbruikende bacteriën kunnen de brandstof van de toekomst zijn
- Eenzame watermoleculen blijken directeuren van supramoleculaire chemie te zijn

 Wie is de heerser van het universum?
Wie is de heerser van het universum?  Wat is een versnellings lichaam?
Wat is een versnellings lichaam?  Hoeveel satellieten heeft India naar de ruimte gestuurd?
Hoeveel satellieten heeft India naar de ruimte gestuurd?  UPS lanceert pakketbezorging per drone
UPS lanceert pakketbezorging per drone Wat de drijvende kracht op een object is gelijk aan het gewicht van water, wat is het?
Wat de drijvende kracht op een object is gelijk aan het gewicht van water, wat is het?  Hoe mieren biogeografische grenzen afbreken en de biodiversiteit homogeniseren
Hoe mieren biogeografische grenzen afbreken en de biodiversiteit homogeniseren  Wat is een nucleaire vergelijking voor Technetium -verval?
Wat is een nucleaire vergelijking voor Technetium -verval?  Hoeveel mol zilvernitraat zou nodig zijn om te reageren met 2,00 natriumfosfaat?
Hoeveel mol zilvernitraat zou nodig zijn om te reageren met 2,00 natriumfosfaat?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


