
Wetenschap
Zuurgraad en basiciteit van chemische verbindingen:Na2S, KCl, LiNO3, K3PO4 uitgelegd
1. Na₂S (natriumsulfide):
* Natrium (Na): Een metaal uit Groep 1, dat een sterke basis vormt.
* Sulfide (S²⁻): De geconjugeerde base van een zwak zuur (H₂S).
Algemeen: Na₂S hydrolyseert tot een basische oplossing.
2. KCl (Kaliumchloride):
* Kalium (K): Een metaal uit Groep 1, dat een sterke basis vormt.
* Chloride (Cl⁻): De geconjugeerde base van een sterk zuur (HCl).
Algemeen: KCl zal een neutrale oplossing vormen.
3. LiNO₃ (lithiumnitraat):
* Lithium (Li): Een metaal uit Groep 1, dat een sterke basis vormt.
* Nitraat (NO₃⁻): De geconjugeerde base van een sterk zuur (HNO₃).
Algemeen: LiNO₃ zal een neutrale oplossing vormen.
4. NH₄ClO₄ (ammoniumperchloraat):
* Ammonium (NH₄⁺): Het geconjugeerde zuur van een zwakke base (NH₃).
* Perchloraat (ClO₄⁻): De geconjugeerde base van een sterk zuur (HClO₄).
Algemeen: NH₄ClO₄ zal hydrolyseren en een zure oplossing vormen.
5. K₃PO₄ (Kaliumfosfaat):
* Kalium (K): Een metaal uit Groep 1, dat een sterke basis vormt.
* Fosfaat (PO₄³⁻): De geconjugeerde base van een zwak zuur (H₃PO₄).
Algemeen: K₃PO₄ hydrolyseert tot een basische oplossing.
Samenvatting:
* Basis: Na₂S, K₃PO₄
* Neutraal: KCl, LiNO₃
* Zuur: NH₄ClO₄
 Hoeveel elementen zitten er in de stofkoolstofdioxide?
Hoeveel elementen zitten er in de stofkoolstofdioxide?  Welk type metaal is niet -untrium?
Welk type metaal is niet -untrium?  Welke zou sneller ijs smelten in een pot met water of kuip warm water?
Welke zou sneller ijs smelten in een pot met water of kuip warm water?  Wat betekent oplossing in de wetenschap?
Wat betekent oplossing in de wetenschap?  Van de drie soorten radioactiviteit die door Rutherford worden gekenmerkt, welke zijn elektrisch geladen A) B-stralen, B) a-stralen en B-stralen?
Van de drie soorten radioactiviteit die door Rutherford worden gekenmerkt, welke zijn elektrisch geladen A) B-stralen, B) a-stralen en B-stralen?
 Fossiele of anorganische structuur? Wetenschappers graven in vroege levensvormen
Fossiele of anorganische structuur? Wetenschappers graven in vroege levensvormen Zijn planten onderdeel van de levenswetenschap?
Zijn planten onderdeel van de levenswetenschap?  Nieuw onderzoek naar Darwins vinken biedt een zeldzaam inzicht in hoe soorten uiteenlopen
Nieuw onderzoek naar Darwins vinken biedt een zeldzaam inzicht in hoe soorten uiteenlopen  Waarom is gevleugelde boon dicot?
Waarom is gevleugelde boon dicot?  Hoe beïnvloedt de relatieve afstand van objecten van de aarde hoe ze verschijnen?
Hoe beïnvloedt de relatieve afstand van objecten van de aarde hoe ze verschijnen?
Hoofdlijnen
- Nieuwe aanwijzingen over hoe poortwachter voor de celkern werkt
- Studie onthult verschillen in belangrijke evoluties van het genoom van gewassen
- Wat zijn resultaten in de wetenschap?
- Wat is de pH van de muisbloed?
- Uitvindingen van de evolutie:wat kikkers een gezicht geeft
- Wat is evolutie van ontwikkelingsadministratie?
- Is bacteriën een plant of dierencel?
- Wat is een unieke rol van organismen in het ecosysteem?
- Wat is uniek aan DNA?
- Wetenschappers ontdekken dat hydratatie de sleutel is tot het verbeteren van de prestaties van katalysatoren voor industrieel gebruik
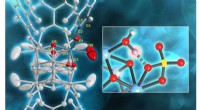
- Bacteriën met metaaldieet ontdekt in vuil glaswerk
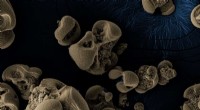
- Metaalkatalysatoren die worden gebruikt voor milieuduurzaamheid blijken te degraderen en worden minder effectief
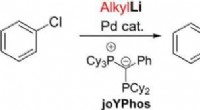
- Directe koppeling van arylhalogeniden en alkyllithiumverbindingen door palladiumkatalyse
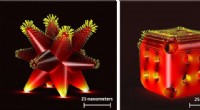
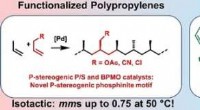
- Katalysatoren voor isotactische polaire polypropylenen
 Orbitale variaties van de aarde en synchrone ijstijden op zee-ijs
Orbitale variaties van de aarde en synchrone ijstijden op zee-ijs Een benzinekettingzaag converteert welke energiebron?
Een benzinekettingzaag converteert welke energiebron?  Wat gebeurt er in de reactie tussen chloorgas en bromide -ionen?
Wat gebeurt er in de reactie tussen chloorgas en bromide -ionen?  Invasie van wijnstokken? Ecoloog kijkt naar het naast elkaar bestaan van bomen en lianen
Invasie van wijnstokken? Ecoloog kijkt naar het naast elkaar bestaan van bomen en lianen  Waarom hebben sommige stoffen wetenschappelijk geen geur?
Waarom hebben sommige stoffen wetenschappelijk geen geur?  Hoe kun je de windrichting bepalen door je vinger nat te maken en deze in de lucht te houden?
Hoe kun je de windrichting bepalen door je vinger nat te maken en deze in de lucht te houden?  Kinderen vertonen al op jonge leeftijd een impliciete raciale houding, onderzoek bevestigt
Kinderen vertonen al op jonge leeftijd een impliciete raciale houding, onderzoek bevestigt Hoe is een planetarium vergelijkbaar met hemelse sfeer?
Hoe is een planetarium vergelijkbaar met hemelse sfeer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

