
Wetenschap
Oxidatiegetallen begrijpen:een praktisch voorbeeld (NaCl)
Voorbeeld van oxidatiegetal:
Laten we de verbinding Natriumchloride (NaCl) nemen
1. Identificeer de elementen: We hebben natrium (Na) en chloor (Cl).
2. Regels toepassen:
* Regel 1: Het oxidatiegetal van een element in zijn elementaire vorm is altijd nul.
* Regel 2: Alkalimetalen (zoals natrium) hebben in verbindingen altijd een oxidatiegetal van +1.
* Regel 3: Halogenen (zoals chloor) hebben gewoonlijk een oxidatiegetal van -1 in verbindingen.
3. Wijs oxidatienummers toe:
* Natrium (Na) heeft een oxidatiegetal van +1 .
* Chloor (Cl) heeft een oxidatiegetal van -1 .
Daarom zijn de oxidatiegetallen in NaCl +1 voor natrium en -1 voor chloor.
Uitleg:
Natrium zit in groep 1, wat betekent dat het één valentie-elektron heeft dat het gemakkelijk opgeeft om een stabiel octet te bereiken. Chloor zit in groep 17 en heeft één elektron nodig om zijn octet te voltooien. Wanneer ze binden, verliest natrium een elektron (wordt +1), en chloor krijgt dat elektron (wordt -1).
Belangrijkste punten:
* Oxidatiegetallen zijn een boekhoudkundig hulpmiddel om de elektronenbeweging in chemische reacties te volgen.
* Het zijn geen werkelijke ladingen, maar eerder een manier om de hypothetische lading weer te geven die een atoom zou hebben als alle bindingen ionisch zouden zijn.
* De som van de oxidatiegetallen in een neutrale verbinding moet gelijk zijn aan nul.
*Het oxidatiegetal van een element kan variëren, afhankelijk van de verbinding waarin het zich bevindt.
 Stapsgewijze handleiding voor het bereiden van een steriele natriumchlorideoplossing
Stapsgewijze handleiding voor het bereiden van een steriele natriumchlorideoplossing  Standaardiseren HCL met behulp van NA2CO3 -titratie. Textbook zegt dat de oplossing op het equivalentiepunt enigszins zuur is. het en waarom?
Standaardiseren HCL met behulp van NA2CO3 -titratie. Textbook zegt dat de oplossing op het equivalentiepunt enigszins zuur is. het en waarom?  Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn
Onderzoeksteam bereikt doorbraak in productie van veelgeprezen kankerbestrijdend medicijn Waarom groeien vloeistoffen en vaste stoffen uit met de temperatuur die niet samendrukbaar is als een gas?
Waarom groeien vloeistoffen en vaste stoffen uit met de temperatuur die niet samendrukbaar is als een gas?  Onderzoekers identificeren meer mogelijke toegangspunten voor COVID-spike-eiwit
Onderzoekers identificeren meer mogelijke toegangspunten voor COVID-spike-eiwit
 Het water van de aarde kan oorspronkelijk diep in de mantel zijn gevormd, studie toont
Het water van de aarde kan oorspronkelijk diep in de mantel zijn gevormd, studie toont Rapport schetst maatregelen om eigenaren van commercieel vastgoed te beschermen tegen overstromingen
Rapport schetst maatregelen om eigenaren van commercieel vastgoed te beschermen tegen overstromingen Wat betekent het woord consumenten in de wetenschap?
Wat betekent het woord consumenten in de wetenschap?  Heeft vegetatiebedekking invloed op de hoeveelheid water in stroomgebieden?
Heeft vegetatiebedekking invloed op de hoeveelheid water in stroomgebieden?  Wetenschapsprojecten met overstromingsmodellen
Wetenschapsprojecten met overstromingsmodellen
Hoofdlijnen
- Hoe handhaaft het plasmamembraan homeostase?
- Wat doet het gen dat Tay Sachs normaal doet?
- Zalmkwekerijen verkeren in een crisis – dit is hoe wetenschappers ze proberen te redden
- Wat is eigenlijk haploïde?
- Welk orgaan produceert lipase?
- Welke bacteriestam ontwikkeld uit natuurlijke isolaten door genetische manipulatie kan worden gebruikt voor de behandeling van olievlekken?
- Altruïsme bij vogels? Eksters zijn wetenschappers te slim af geweest door elkaar te helpen trackingapparaten te verwijderen
- Experimenten tonen aan dat de gegevens over het vroege leven volledig 'vals-positieven' kunnen zijn
- Welke term wordt gebruikt voor de combinatie van twee niet -cellulaire componenten bindweefsel?
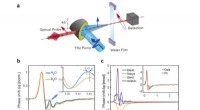
- Ultrasnelle waterstofbrugdynamiek van vloeibaar water onthuld door THz-geïnduceerd Kerr-effect
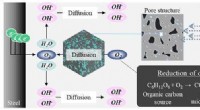
- Corrosiebestendigheid van stalen staven in beton bij vermenging met aerobe micro-organismen
- Wetenschappers suggereren een milieuvriendelijke manier om zeer actieve katalysatoren te verkrijgen

- Procesmodellering voor efficiëntere pulp- en papierproductie

- Een nieuwe microscoop onthult het wonder van moleculaire zuurstof

 Wat zijn enkele kenmerken van metalen?
Wat zijn enkele kenmerken van metalen?  JPL zet een CubeSat in voor astronomie
JPL zet een CubeSat in voor astronomie De toekomst van energievoorziening:gecombineerde energieopslag een sleuteltechnologie
De toekomst van energievoorziening:gecombineerde energieopslag een sleuteltechnologie Hoe laat komt New Moon uit?
Hoe laat komt New Moon uit?  Wat zijn de gemeenschappelijke energiedragers in de cel?
Wat zijn de gemeenschappelijke energiedragers in de cel?  Eerste gezamenlijke Frankrijk-China-satelliet om oceanen te bestuderen
Eerste gezamenlijke Frankrijk-China-satelliet om oceanen te bestuderen Hoe maak je een lift voor een Science Fair-project
Hoe maak je een lift voor een Science Fair-project  Welke lagen van de aarde toenemen met dichtheid?
Welke lagen van de aarde toenemen met dichtheid?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

