
Wetenschap
Metaaloxidatie en metaalchloriden begrijpen:een chemische afbraak
* Reactanten:
* Metaal: Elk metaal kan reageren met zuurstof. Veel voorkomende voorbeelden zijn ijzer (Fe), koper (Cu), aluminium (Al) en magnesium (Mg).
* Zuurstof (O2): Dit is een diatomisch gas dat in de lucht wordt aangetroffen.
* Producten:
* Metaaloxide: Dit is het primaire product. Het metaal combineert met zuurstof en vormt een verbinding met de algemene formule MO , waarbij M het metaal vertegenwoordigt.
* Metaalchloride: Dit is *niet* een direct product van de reactie tussen een metaal en zuurstof. Om een metaalchloride te vormen, moet je het metaal laten reageren met chloor (Cl2), en niet met zuurstof.
Voorbeelden:
* IJzer (Fe) + Zuurstof (O2) → IJzer(III)oxide (Fe2O3) (Roest)
* Koper (Cu) + zuurstof (O2) → Koper(II)oxide (CuO)
* Magnesium (Mg) + Zuurstof (O2) → Magnesiumoxide (MgO)
Belangrijke opmerking: Metaaloxiden zijn vaak het gevolg van corrosie of oxidatie van metalen, een natuurlijk proces dat in de loop van de tijd plaatsvindt wanneer metalen worden blootgesteld aan lucht en water.
Hoofdlijnen
- Waarom zijn de meeste cellen klein?
- Wat hebben bacteriën gemeen met cellen en andere levende organismen?
- Waarom zijn de vrije nucleotiden belangrijk voor levende cellen?
- Op welk substraat werkt speeksel amylase?
- Octopussen gestrand op het strand van Wales - hier zijn de wetenschappelijke theorieën waarom
- Definieer wat een geïntroduceerde soort is?
- In welke staten dat elk genpaar onafhankelijk van de paren wordt geërfd voor andere eigenschappen?
- Zijn dinosaurussen echt? Wat we weten over de uitgestorven wezens
- Vijf veerkrachtige soorten die conventionele moordmethoden trotseren
- Het stabiliseren van emulsieonderzoek verbetert de brandbestrijding en meer

- Nieuwe chemische mechanismen geïdentificeerd op weg naar schoner, efficiëntere verbranding

- Een radicale oplossing komt van het mengen van gereedschappen

- Wetenschappers rekruteren nieuwe atoomzwaargewichten in gerichte strijd tegen kanker

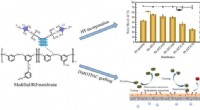
- Nieuwe technologie om de hoge permselectiviteit en anti-biofouling eigenschappen van RO-membranen te verbeteren
 Atomaire reactiviteit begrijpen:de rol van elektronen
Atomaire reactiviteit begrijpen:de rol van elektronen  Turbulentie verwondt 30 gewonden op vlucht van Istanbul naar New York
Turbulentie verwondt 30 gewonden op vlucht van Istanbul naar New York Wat gebeurt er wanneer een elektrische stroom wordt gemaakt door een veranderend magnetisch veld?
Wat gebeurt er wanneer een elektrische stroom wordt gemaakt door een veranderend magnetisch veld?  Wat is maximale snelheid in HDPE -pijp?
Wat is maximale snelheid in HDPE -pijp?  Diepgaand leren voor glaucoomdetectie
Diepgaand leren voor glaucoomdetectie Welk percentage van de naties energie wordt verstrekt door thermisch?
Welk percentage van de naties energie wordt verstrekt door thermisch?  Top 5 dingen die u kunt doen om groener te rekenen
Top 5 dingen die u kunt doen om groener te rekenen  Wat is de lading van polyatomische ionen nitraat en chloriet?
Wat is de lading van polyatomische ionen nitraat en chloriet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


