
Wetenschap
Hoe oplosmiddelen ionische verbindingen oplossen:een gedetailleerde uitleg
Hier is een overzicht:
* Ionische verbindingen: Deze verbindingen zijn samengesteld uit positief geladen kationen en negatief geladen anionen die bij elkaar worden gehouden door sterke elektrostatische krachten.
* Oplosmiddelen: Oplosmiddelen zijn stoffen die andere stoffen kunnen oplossen. Polaire oplosmiddelen hebben, net als water, moleculen met een positief en negatief uiteinde (dipool) vanwege de ongelijke verdeling van elektronen.
* Oplossingsproces: Wanneer een polair oplosmiddel zoals water een ionische verbinding tegenkomt, trekt het positieve uiteinde van het watermolecuul de negatieve ionen (anionen) van de ionische verbinding aan, en het negatieve uiteinde van het watermolecuul trekt de positieve ionen (kationen) aan. Deze aantrekkingskracht verzwakt de elektrostatische krachten die de ionen in de vaste stof bij elkaar houden.
* Hydratatie (of solvatie): De watermoleculen omringen vervolgens de individuele ionen en vormen een hydratatiesfeer. Dit proces, solvatatie genoemd, isoleert de ionen effectief van elkaar en voorkomt dat ze het ionenrooster opnieuw vormen. Het resultaat is dat de ionische verbinding oplost.
Belangrijkste punten om te onthouden:
* Polaire oplosmiddelen zijn over het algemeen beter in het oplossen van ionische verbindingen dan niet-polaire oplosmiddelen.
* De sterkte van de elektrostatische krachten tussen ionen in de ionische verbinding beïnvloedt de oplosbaarheid ervan. Sterkere krachten leiden tot een lagere oplosbaarheid.
* De polariteit van het oplosmiddel beïnvloedt zijn vermogen om met de ionen te interageren en ze uit elkaar te halen.
Laat het me weten als je nog vragen hebt!
 Wat is de toekomst van kernenergie?
Wat is de toekomst van kernenergie?  Verandering van omgeving:nieuw onderzoek schetst hoe recreatie zal veranderen als gevolg van de klimaatverandering in het westen
Verandering van omgeving:nieuw onderzoek schetst hoe recreatie zal veranderen als gevolg van de klimaatverandering in het westen  Team waarschuwt dat technologieën voor negatieve emissies de klimaatcrisis mogelijk niet oplossen
Team waarschuwt dat technologieën voor negatieve emissies de klimaatcrisis mogelijk niet oplossen Fototropisme in planten:groei naar licht uitgelegd
Fototropisme in planten:groei naar licht uitgelegd  Lijst met kleine insecten
Lijst met kleine insecten
Hoofdlijnen
- Hoe vaak komt agressie bij Britse honden voor?
- Cel bevat receptor -eiwitten voor verschillende chemicaliën?
- Komt neutralisatie in planten op de wortels?
- Bevat een planten- of diercellen chloroplasten?
- Welke twee dingen hebben dieren in hun cellen nodig om ademhaling uit te voeren?
- Wat produceert eiwitten door gecodeerde instructies van de kern te volgen?
- Wat betekent onderzoek in de wetenschap?
- Wat zorgen voor koolhydraten voor de cel?
- Het oplossen van de evolutionaire geschiedenis van de naaste verwanten van algen van landplanten
- Bindingsmechanisme met eenmaal korting kan de sleutel zijn om virussen te targeten
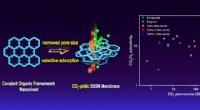
- Eenfasige covalente organische raamwerkmembranen maken CO2-selectieve scheiding mogelijk
- Unieke constructies maken van metalen membranen

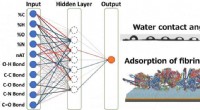
- Een sprong voorwaarts voor het ontwerpen van biomaterialen met AI
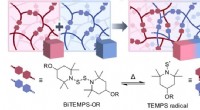
- Het onvermengbare mengen:een nieuwe benadering voor het efficiënt samensmelten van verschillende polymeren
 Kenmerken van een omgeving die niet leeft, zoals bodemwater en klimaatfactoren?
Kenmerken van een omgeving die niet leeft, zoals bodemwater en klimaatfactoren?  Wat is de afgeleide van benzoëzuur?
Wat is de afgeleide van benzoëzuur?  Toiletpapier, handreinigingsmiddel, en nu elastisch? Maskersmakers gaan om met onverwachte COVID-19-gerelateerde tekorten
Toiletpapier, handreinigingsmiddel, en nu elastisch? Maskersmakers gaan om met onverwachte COVID-19-gerelateerde tekorten Kankerdiagnostische bedrijven sluiten zich aan bij een deal van $ 2,8 miljard
Kankerdiagnostische bedrijven sluiten zich aan bij een deal van $ 2,8 miljard Welke 3 dingen maken planten als ze door fotosynthese gaan?
Welke 3 dingen maken planten als ze door fotosynthese gaan?  Wat is de relatie tussen massa en snelheid van een object in uniforme versnelling?
Wat is de relatie tussen massa en snelheid van een object in uniforme versnelling?  Edelmetaal volgt nanoplastics
Edelmetaal volgt nanoplastics Wat zijn enkele items die gelijk zijn aan de Ozone vernietigen?
Wat zijn enkele items die gelijk zijn aan de Ozone vernietigen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

