
Wetenschap
Dubbele covalente binding tussen zuurstofatomen:uitleg en vorming
* Elektronische configuratie van zuurstof: Zuurstof heeft zes elektronen in de buitenste schil (valentieschil). Er zijn nog twee elektronen nodig om een stabiel octet (acht elektronen) te bereiken.
* Elektronen delen: Om deze stabiliteit te bereiken delen twee zuurstofatomen twee elektronenparen, waardoor een dubbele covalente binding ontstaat. Door dit delen kan elk zuurstofatoom acht elektronen in zijn buitenste schil hebben.
Vertegenwoordiging:
De dubbele covalente binding tussen twee zuurstofatomen wordt vaak als volgt weergegeven:
O=O
Deze notatie laat zien dat twee elektronenparen worden gedeeld tussen de twee zuurstofatomen.
 Stapsgewijze handleiding voor het tekenen van een calciumchloride-omhulselmodel
Stapsgewijze handleiding voor het tekenen van een calciumchloride-omhulselmodel  Wat zijn de voordelen voor het construeren van modellen van moleculen in tegenstelling tot het tekenen van ze?
Wat zijn de voordelen voor het construeren van modellen van moleculen in tegenstelling tot het tekenen van ze?  Wat is de functie van natriumchloride?
Wat is de functie van natriumchloride?  Aluminium- en zinknitraatreactie:het chemische proces begrijpen
Aluminium- en zinknitraatreactie:het chemische proces begrijpen  Je hebt 0,2 n kmno4 en je moet het 0,05 n verdunnen, hoe kan dat?
Je hebt 0,2 n kmno4 en je moet het 0,05 n verdunnen, hoe kan dat?
Hoofdlijnen
- Waar kan wetenschap voor worden gebruikt?
- Welk koninkrijk heeft slechts één cel maar geen kern in het midden?
- Exogeen RNA:definitie, bronnen en biologische betekenis
- Beschrijf de kenmerken van Miss Phatuphats en leg uit?
- Welke soorten weefsels vormen de buitenafhankelijke en lijnen organen dieren?
- Een interactie in welke het ene organisme vangt en zich op een ander voedt, wordt opgeroepen?
- Zijn mensen een product van puntmutatie?
- Wat betekent wetenschappelijk?
- Experiment onthult strategisch denken bij muizen
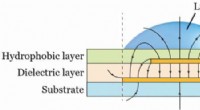
- Een nieuwe kijk op kleurendisplays

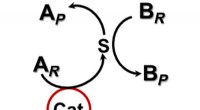
- Chemische reacties versnellen zonder direct contact met een katalysator
- Fasegescheiden eiwitachtige lijmen als zelforganizer van microfilamentnetwerken

- Hydrogel 3D-print- en patroonvloeistoffen met het condensatorrandeffect (PLEEC)
- De algehele reactievolgorde begrijpen:hoe concentratie de reactiesnelheid beïnvloedt

 Wat is de geleider van de wetenschapsdefinitie?
Wat is de geleider van de wetenschapsdefinitie?  Breuken op een getallenlijn plaatsen
Breuken op een getallenlijn plaatsen Wat doet chloroplasten in je lichaam?
Wat doet chloroplasten in je lichaam?  Elementen bevatten met elektronen in S P D- en F -orbitalen?
Elementen bevatten met elektronen in S P D- en F -orbitalen?  Welk type binding vormt arseen?
Welk type binding vormt arseen?  Hoe zijn selectief permeabele membranen essentieel voor het leven?
Hoe zijn selectief permeabele membranen essentieel voor het leven?  Wat zijn de doelstellingen van zuur?
Wat zijn de doelstellingen van zuur?  Nieuw mineraal, priscillagrewite, genoemd ter ere van de beroemde geoloog van Nebraska
Nieuw mineraal, priscillagrewite, genoemd ter ere van de beroemde geoloog van Nebraska
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

