
Wetenschap
Zuren begrijpen:definities en voorbeelden (Arrhenius &Brønsted-Lowry)
Arrhenius-definitie:
* Een zuur is een stof die waterstofionen (H+) produceert wanneer deze in water wordt opgelost.
* Voorbeelden:HCl (zoutzuur), HNO3 (salpeterzuur), H2SO4 (zwavelzuur)
Brønsted-Lowry-definitie:
* Een zuur is een stof die een proton (H+) kan doneren aan een andere stof (een base).
* Deze definitie is algemener dan de Arrhenius-definitie, aangezien deze van toepassing is op reacties in andere oplosmiddelen dan water.
* Voorbeelden:HCl, HNO3, H2SO4, evenals organische zuren zoals azijnzuur (CH3COOH)
Lewis-definitie:
* Een zuur is een stof die een elektronenpaar van een andere stof (een base) kan accepteren.
* Dit is de breedste definitie en omvat alle zuren in de definities van Arrhenius en Brønsted-Lowry, en omvat ook stoffen die geen waterstofatomen bevatten.
* Voorbeelden:BF3 (boortrifluoride), AlCl3 (aluminiumchloride)
Belangrijkste eigenschappen van zuren:
* Zure smaak: Dit is hoe zuren voor het eerst werden geïdentificeerd.
* Reageren met basen om zout en water te vormen: Dit staat bekend als neutralisatie.
* Maak blauw lakmoespapier rood: Dit is een klassieke test voor zuren.
* Geleid elektriciteit: Dit komt omdat zuren in water dissociëren en ionen vormen, die een elektrische stroom kunnen geleiden.
Belangrijke opmerking: Zuren zijn bijtend en kunnen gevaarlijk zijn als ze niet op de juiste manier worden behandeld. Draag altijd beschermende kleding wanneer u met zuren werkt en volg veiligheidsprotocollen.
 Zijn conserveermiddelen een zuur of een base?
Zijn conserveermiddelen een zuur of een base?  Onderzoekers ontwikkelen hybride superamfifobe anticorrosie- en anti-ijsvormingscoating
Onderzoekers ontwikkelen hybride superamfifobe anticorrosie- en anti-ijsvormingscoating  Als het smeltpunt 112c is, is dit dan een fysische of chemische eigenschap van zwavel?
Als het smeltpunt 112c is, is dit dan een fysische of chemische eigenschap van zwavel?  Wat is Acidity Regulator 338?
Wat is Acidity Regulator 338?  Wat bepaalt in hoeverre een proton-overdrachtsreactie optreedt?
Wat bepaalt in hoeverre een proton-overdrachtsreactie optreedt?
 Suomi NPP vindt ongeorganiseerde stormen in tropische depressie 29W
Suomi NPP vindt ongeorganiseerde stormen in tropische depressie 29W Guatemala leeft al eeuwen in de schaduw van vulkanen
Guatemala leeft al eeuwen in de schaduw van vulkanen In een opwarmende wereld, Cape Towns Day Zero droogte zal geen anomalie zijn
In een opwarmende wereld, Cape Towns Day Zero droogte zal geen anomalie zijn Google Street View-auto's zijn ogen op de grond voor stedelijke methaanlekken
Google Street View-auto's zijn ogen op de grond voor stedelijke methaanlekken Wat veroorzaakt getijden? Hoog- en laagwater uitgelegd
Wat veroorzaakt getijden? Hoog- en laagwater uitgelegd
Hoofdlijnen
- Wat is de basiseenheid van reproductie?
- Wat is een bacteriofheophytine?
- De nieuwste meren van Alaska boeren methaan op
- Welke soorten organismen hebben gespecialiseerde cellen?
- Hoe lijken mitochondriën en chloroplasten op bacteriën?
- Een taxonomische categorie tussen koninkrijk en klasse is.
- Wat is biotictechnologie?
- Hoe beschrijft u hoe bloedgroepen voorbeelden zijn van multiple allelen en codominantie?
- Japanse dierentuin rouwt om dood van verliefde pinguïn
- De oorsprong van oppervlakteruwheid:atoomvervorming binnen en op het oppervlak van een vaste stof

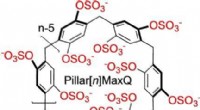
- Moleculaire containers voor de sekwestratie van neurotransmittergeneesmiddelen in water
- Techniekteam maakt monitoringtoolkit om de productie van biologische medicijnen te versnellen

- Elektriciteit gebruiken om verbindingen te maken voor farmaceutische producten, andere chemicaliën

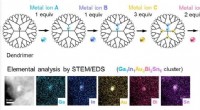
- Doorbraak in het mengen van metalen - nauwkeurige controle van multimetallische clustervorming van één nanometer bereikt
 Hoeveel atomen zijn er in 3,91 mol natrium?
Hoeveel atomen zijn er in 3,91 mol natrium?  Waarom vertelt de Dopplerverschuiving ons alleen over beweging direct langs de zichtlijn tussen een lichtbron en een waarnemer, maar niet over de hemelbol?
Waarom vertelt de Dopplerverschuiving ons alleen over beweging direct langs de zichtlijn tussen een lichtbron en een waarnemer, maar niet over de hemelbol?  Hoe breuken in DNA worden gerepareerd
Hoe breuken in DNA worden gerepareerd  Wat is een echt diagram?
Wat is een echt diagram?  Wat zijn processen van wetenschap of wetenschappelijke processen?
Wat zijn processen van wetenschap of wetenschappelijke processen?  Klimaatverandering:boomopstanden van gemengde soorten passen zich beter aan dan zuivere opstanden
Klimaatverandering:boomopstanden van gemengde soorten passen zich beter aan dan zuivere opstanden Wat kan er gebeuren voor een beperkte genenstroom?
Wat kan er gebeuren voor een beperkte genenstroom?  Is het waar dat de vrouwen uit Planet Venus komen?
Is het waar dat de vrouwen uit Planet Venus komen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

