
Wetenschap
Zuur-basereacties:oxide- en waterreacties begrijpen
* Zuur: Zuren doneren waterstofionen (H+) in oplossing.
* Niet-metaaloxide: Niet-metaaloxiden zijn zure oxiden, wat betekent dat ze reageren met water om zuren te vormen.
* Water: Water fungeert als oplosmiddel, waardoor het zuur en het niet-metaaloxide kunnen reageren.
Hoe het werkt:
1. Niet-metaaloxide reageert met water: Het niet-metaaloxide lost op in water en vormt een zuur. Bijvoorbeeld:
* CO₂ (kooldioxide) + H₂O (water) → H₂CO₃ (koolzuur)
2. Zuur reageert met het zuur gevormd in stap 1: Het oorspronkelijke zuur neutraliseert het zuur gevormd uit het niet-metaaloxide. Hierbij reageren de waterstofionen (H+) uit het oorspronkelijke zuur met de anionen (negatieve ionen) uit het zuur gevormd uit het niet-metaaloxide.
* HCl (zoutzuur) + H₂CO₃ (koolzuur) → H₂O (water) + CO₂ (kooldioxide) + 2Cl⁻ (chloride-ionen)
Over het geheel genomen kan de reactie als volgt worden samengevat:
Zuur + niet-metaaloxide + water → zout + water
Voorbeeld:
* HCl (zoutzuur) + SO₂ (zwaveldioxide) + H₂O (water) → H₂SO₄ (zwavelzuur) + H₂O (water)
Hier reageert zwaveldioxide (SO₂) met water en vormt zwavelzuur (H₂SO₃). Vervolgens reageert zoutzuur (HCl) met zwavelzuur en vormt water, zwavelzuur (H₂SO₄) en chloride-ionen (Cl⁻).
Belangrijke opmerkingen:
* Niet alle niet-metaaloxiden reageren met water. Sommige, zoals koolmonoxide (CO), zijn relatief niet-reactief.
* De specifieke producten zijn afhankelijk van de identiteit van het zuur en het niet-metaaloxide.
Laat het me weten als je specifieke voorbeelden wilt verkennen of als je nog vragen hebt!
 Sneeuwvalpatronen kunnen aanwijzingen geven voor de Groenlandse ijskap
Sneeuwvalpatronen kunnen aanwijzingen geven voor de Groenlandse ijskap Bomen in dit biome werpen hun bladeren af. De herfsttemperatuur varieert met seizoenen is de?
Bomen in dit biome werpen hun bladeren af. De herfsttemperatuur varieert met seizoenen is de?  Zullen voedselketens breken naarmate de seizoenen onvoorspelbaarder worden?
Zullen voedselketens breken naarmate de seizoenen onvoorspelbaarder worden?  Satelliet toont wat afschuiving in orkaan Hilary
Satelliet toont wat afschuiving in orkaan Hilary Waarom is het regenwoud vochtig?
Waarom is het regenwoud vochtig?
Hoofdlijnen
- Onderzoek laat zien hoe mariene bacteriën algen bestrijden
- Welk cellulair proces vindt plaats in de ribosomen die gebonden zijn aan endoplasmatisch reticulum?
- De elektronentransportketens van cellulaire ademhaling bevinden zich?
- Leg uit hoe de nucleolus bijdraagt aan eiwitsynthese?
- Multiresistente genetische factoren bij malariaparasieten
- Wat is een vetzuur? | Hoe dingen werken
- Om aminozuren te creëren, vereist de genetische code nucleotiden?
- Functie van lysosomen in een cel?
- Welke verschillen zouden worden verwacht in experimenten met squash die niet zelf bestuiven?
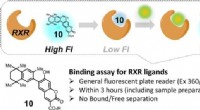
- Synthetische verbinding zorgt voor snelle screening op potentiële medicijnen
- Nieuwe aanpak voor het opvangen van gas bevordert het beheer van nucleaire brandstof

- Hoe hitte en zonlicht het chloorniveau in het zwembad beïnvloeden

- Modificatie van aminozuren biedt nieuw startpunt voor ontwikkeling van medische behandelingen

- Wetenschappers ontwikkelen een cellulose-biosensormateriaal voor geavanceerde weefseltechnologie
 Op hoeveel manieren kan de zon ons helpen elektriciteit te produceren?
Op hoeveel manieren kan de zon ons helpen elektriciteit te produceren?  Zware regen in het noorden van Japan, 200.000 mensen moeten evacueren
Zware regen in het noorden van Japan, 200.000 mensen moeten evacueren De vulkanische activiteit van Mercurius - of het gebrek daaraan - kan astronomen helpen andere aardachtige werelden te vinden
De vulkanische activiteit van Mercurius - of het gebrek daaraan - kan astronomen helpen andere aardachtige werelden te vinden Een kristallen bruiloft in de nanokosmos
Een kristallen bruiloft in de nanokosmos Hoe verschillen bacteriecellen van de eukaryoten?
Hoe verschillen bacteriecellen van de eukaryoten?  Lasers maken miniatuurrobots van bubbels
Lasers maken miniatuurrobots van bubbels Wat irriteert een chimpansee?
Wat irriteert een chimpansee? Welk proces geeft een broek energie vrij uit opgeslagen voedsel?
Welk proces geeft een broek energie vrij uit opgeslagen voedsel?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

