
Wetenschap
Zwaar water (D₂O):eigenschappen, toepassingen en verschillen met gewoon water
Dit is waarom:
* Deuterium is een isotoop van waterstof, wat betekent dat het hetzelfde aantal protonen (1) heeft, maar een ander aantal neutronen (1 voor deuterium, 0 voor protium). Dit maakt deuterium zwaarder dan protium.
* Zwaar water is chemisch vergelijkbaar met gewoon water (H₂O), maar de waterstofatomen zijn vervangen door deuteriumatomen (²H of D), waardoor D₂O ontstaat.
Belangrijkste punten om te onthouden over zwaar water:
*Het is zwaarder dan gewoon water vanwege het extra neutron in deuterium.
*Het heeft andere fysische eigenschappen vergeleken met gewoon water (bijvoorbeeld hoger kookpunt, lager vriespunt).
*Het kan in grote hoeveelheden giftig zijn, omdat het biologische processen verstoort.
* Het wordt gebruikt in kernreactoren en wetenschappelijk onderzoek.
 Is normale zoutoplossing met 20 procent kcl een hypertone oplossing?
Is normale zoutoplossing met 20 procent kcl een hypertone oplossing?  Waarom hebben verschillende vloeistoffen een viswaardigheid?
Waarom hebben verschillende vloeistoffen een viswaardigheid?  Wetenschappers synthetiseren een materiaal dat zenuwgassen in water kan afbreken
Wetenschappers synthetiseren een materiaal dat zenuwgassen in water kan afbreken Welke stof is correct gekoppeld aan het type binding br2 polair covalent?
Welke stof is correct gekoppeld aan het type binding br2 polair covalent?  Hoe scheid je ijzervullingen van babypoeder?
Hoe scheid je ijzervullingen van babypoeder?
 Waarom hebben we scherpere weer- en klimaatmodellen nodig?
Waarom hebben we scherpere weer- en klimaatmodellen nodig?  Bedreigde soorten in de Afrikaanse savanne
Bedreigde soorten in de Afrikaanse savanne  Verwachte verzuring van het Great Barrier Reef kan met tien jaar worden gecompenseerd
Verwachte verzuring van het Great Barrier Reef kan met tien jaar worden gecompenseerd Stam in de buurt van de grootste stad van Brazilië vecht om vol te houden
Stam in de buurt van de grootste stad van Brazilië vecht om vol te houden Ontbossing verduistert de zeeën boven het op een na grootste rif ter wereld
Ontbossing verduistert de zeeën boven het op een na grootste rif ter wereld
Hoofdlijnen
- Welke van deze monitoren de pH-waarden in het bloed?
- Wat is de naam van nakomelingen twee verschillende soorten?
- Waarom is het belangrijk voor de wetenschap en de samenleving om te communiceren over stamcellen?
- Nieuwe mechanismen beschrijven hoe het genoom zichzelf reguleert
- Welke cel wordt waargenomen als A de vorming van een contractiele ring vertoont net voorafgaand aan cytoplasmatische divisie?
- Semantisch gesproken:verenigt betekenisstructuur talen?
- Welke theorie verbindt de velden van biologie en geologie samen?
- Wetenschappers bewerken vlindervleugelvlekken en strepen
- Indringende vraag:Waarom overleefden zoogdieren het 'K/T-uitsterven'?
- Duurzaam waterzuiveringssysteem geïnspireerd door de natuur

- Drugsbibliothecaris ontdekt nieuwe stof die veelvoorkomende chirurgische complicaties kan dwarsbomen
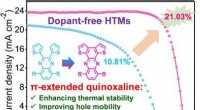
- Doteringsvrij, vochtstabiele organische lagen geven perovskiet-zonnecellen 21% efficiëntie
- Krachtige antimicrobiële gevonden die veelbelovend is in het bestrijden van stafylokokbesmettingen

- Wetenschappers bedenken snellere manier om antibiotica te ontdekken

 Bovenaan een piramide biomassa staan de?
Bovenaan een piramide biomassa staan de?  Waarom de witte vlieg zo'n formidabele bedreiging vormt voor de voedselzekerheid
Waarom de witte vlieg zo'n formidabele bedreiging vormt voor de voedselzekerheid  Delen van een telescoop
Delen van een telescoop  Zijn nucleïnezuren oplosbaar in water?
Zijn nucleïnezuren oplosbaar in water?  Waarom gloeien sommige boomwortels in het donker als ze worden blootgesteld?
Waarom gloeien sommige boomwortels in het donker als ze worden blootgesteld?  Een nieuwe benadering voor softwarefoutvoorspelling met behulp van functieselectie
Een nieuwe benadering voor softwarefoutvoorspelling met behulp van functieselectie De zoektocht naar nieuwe materialen voor waterstofopslag
De zoektocht naar nieuwe materialen voor waterstofopslag Oude uitwerpselen onthullen hoe 'moerasdieet' de Vennen uit de Bronstijd met parasieten besmette
Oude uitwerpselen onthullen hoe 'moerasdieet' de Vennen uit de Bronstijd met parasieten besmette
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

