
Wetenschap
Kationen:meer dan 2 geladen ionen en hun voorbeelden begrijpen
Groep 2-elementen (aardalkalimetalen)
* Calcium (Ca²⁺) - Gevonden in botten, tanden en speelt een rol bij spiercontractie.
* Magnesium (Mg²⁺) - Gevonden in chlorofyl, essentieel voor fotosynthese.
* Barium (Ba²⁺) - Gebruikt in vuurwerk voor groene kleur.
* Strontium (Sr²⁺) - Gebruikt in vuurwerk voor rode kleur.
Overgangsmetalen
* IJzer (Fe²⁺) - Aanwezig in hemoglobine, verantwoordelijk voor het zuurstoftransport.
* Koper (Cu²⁺) - Gebruikt in elektrische bedrading en loodgieterswerk.
* Zink (Zn²⁺) - Belangrijk voor de immuunfunctie en wondgenezing.
* Mangaan (Mn²⁺) - Betrokken bij de stofwisseling en botvorming.
Andere voorbeelden
* Lood (Pb²⁺) - Een giftig zwaar metaal.
* Kwik (Hg²⁺) - Een giftig zwaar metaal.
* Nikkel (Ni²⁺) - Gebruikt in batterijen en legeringen.
* Kobalt (Co²⁺) - Gevonden in vitamine B12.
Hoe de lading van een ion bepalen:
* Groep 1 Elementen (Alkalimetalen): +1 lading
* Groep 2 elementen (aardalkalimetalen): +2 opladen
* Halogenen (Groep 17): -1 lading
* Zuurstof (Groep 16): -2 kosten
* Overgangsmetalen: Variërende ladingen, vaak bepaald door de verbinding die ze vormen.
Het is belangrijk op te merken dat de lading van een ion kan worden bepaald door zijn positie op het periodiek systeem en zijn elektronenconfiguratie.
 Wat gebeurt er met atomen van een stof wanneer warmte wordt toegevoegd?
Wat gebeurt er met atomen van een stof wanneer warmte wordt toegevoegd?  Hoe 180 graden metrisch in Fahrenheit te converteren
Hoe 180 graden metrisch in Fahrenheit te converteren  Stabiele radicalen kunnen onconventionele problemen in de moderne wetenschap en technologie oplossen
Stabiele radicalen kunnen onconventionele problemen in de moderne wetenschap en technologie oplossen Hoeveel dingen zitten er in een sigaret?
Hoeveel dingen zitten er in een sigaret?  het verschil tussen freon en ammoniak?
het verschil tussen freon en ammoniak?
Hoofdlijnen
- Een elektronenmicroscoop wordt meestal gebruikt voor micro -organismen die zijn?
- Veel meer bacteriën hebben elektrisch geleidende filamenten
- Wat is de voorlopige hypothese?
- Wat is het doel van ATP -synthetase?
- Waarom is de Palisade -cel speciaal?
- Wat is basis van de natuur aminozuren?
- Wordt een nucleolus gevonden in bacteriecellen?
- Systeem van membranen die helpen stoffen door een cel te verplaatsen?
- Een eenvoudig diermodel laat zien hoe omgeving en toestand worden geïntegreerd om gedrag te controleren
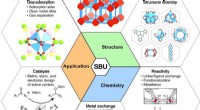
- Secundaire bouweenheden (SBU's) - het keerpunt in de ontwikkeling van metaal-organische raamwerken (MOF's)
- Een lasergestuurde programmeerbare contactloze transferdruktechniek

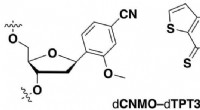
- Halfsynthetische bacteriën produceren onnatuurlijke eiwitten
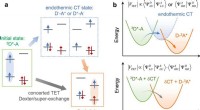
- Endotherme ladingsoverdracht bemiddelt ondiepe afstandsafhankelijke triplet-energiemigratie
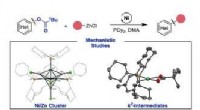
- Katalytische koppelingen begrijpen:niet alle synergieën zijn eenvoudig
 Wat is het doel van de levensvatbaarheid van zaad?
Wat is het doel van de levensvatbaarheid van zaad?  Blijven of verdwalen? Studie duikt in seksueel gedrag
Blijven of verdwalen? Studie duikt in seksueel gedrag  Welke mRNA-streng zou worden gemaakt tijdens transcriptie met behulp van het DNA dat hieronder wordt weergegeven AGC GCT?
Welke mRNA-streng zou worden gemaakt tijdens transcriptie met behulp van het DNA dat hieronder wordt weergegeven AGC GCT?  Hoe druk je 24 voet 11 inch in decimalen uit?
Hoe druk je 24 voet 11 inch in decimalen uit?  Onderzoekers wekken elektriciteit op uit virussen
Onderzoekers wekken elektriciteit op uit virussen Paddenstoelenleer kan de sleutel zijn tot duurzame mode
Paddenstoelenleer kan de sleutel zijn tot duurzame mode Wat zijn de componenten die betrokken zijn bij transcriptie?
Wat zijn de componenten die betrokken zijn bij transcriptie?  Wat is 9 uur Pacific Time in Eastern Daylight Savings Time?
Wat is 9 uur Pacific Time in Eastern Daylight Savings Time?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

