
Wetenschap
Calciumchloride:Ionische bindingen en chemische structuur begrijpen
* Elektrostatische aantrekkingskracht: Calcium (Ca) is een metaal en heeft de neiging twee elektronen te verliezen om een positief ion (Ca²⁺) te vormen. Chloor (Cl) is een niet-metaal en heeft de neiging één elektron te winnen en een negatief ion (Cl⁻) te vormen. De sterke elektrostatische aantrekkingskracht tussen de positief geladen calciumionen en de negatief geladen chloride-ionen vormt de ionische binding.
* Verschil in elektronegativiteit: Het elektronegativiteitsverschil tussen calcium (1,0) en chloor (3,0) is groot (2,0), wat duidt op een overdracht van elektronen in plaats van delen.
* Structuur: Ionische verbindingen vormen doorgaans kristallijne structuren vanwege de regelmatige rangschikking van ionen in een rooster. Calciumchloride vormt een kristalrooster met calciumionen omgeven door chloride-ionen.
Samengevat: Het grote elektronegativiteitsverschil, de vorming van ionen en de kristalstructuur wijzen allemaal op een ionische binding in calciumchloride.
 Nieuw materiaal met sterke werking tegen schimmels en tumoren ontwikkeld
Nieuw materiaal met sterke werking tegen schimmels en tumoren ontwikkeld Licht stimuleert een nieuwe wending in de synthetische chemie
Licht stimuleert een nieuwe wending in de synthetische chemie  Bereken de molaire oplosbaarheid van AGBR in een 3,0 x 10-2 m zilvernitraat AGNO3-oplossing?
Bereken de molaire oplosbaarheid van AGBR in een 3,0 x 10-2 m zilvernitraat AGNO3-oplossing?  Welk deeltje draagt een verwaarloosbare hoeveelheid bij aan de atomaire massa?
Welk deeltje draagt een verwaarloosbare hoeveelheid bij aan de atomaire massa?  Wat is de vergelijking voor ijzer III -chloride plus zilvernitraat?
Wat is de vergelijking voor ijzer III -chloride plus zilvernitraat?
 Wat is het brood der schimmels?
Wat is het brood der schimmels?  Hoe groene mijnbouw de weg kan banen naar netto nul en een duurzame toekomst
Hoe groene mijnbouw de weg kan banen naar netto nul en een duurzame toekomst Hoe beïnvloeden bomen het weer?
Hoe beïnvloeden bomen het weer?  Australisch gas - tussen een gebroken rots en een sociaal moeilijke plek
Australisch gas - tussen een gebroken rots en een sociaal moeilijke plek Wat zijn concepten die beschrijven hoe iemand over iets in de natuurlijke wereld denkt?
Wat zijn concepten die beschrijven hoe iemand over iets in de natuurlijke wereld denkt?
Hoofdlijnen
- Multicellulaire nucleated heterotrofen die altijd voedsel verkrijgen door voedingsstoffen uit de omgeving te absorberen behoren tot welk koninkrijk?
- Noem de structuur die sensorisch ganglion is van elke dorsale wortel?
- Wat zijn de gespecialiseerde cellen en weefsels van het uitscheidingssysteem Wat hun functie?
- Wat bevatten prokaryotische cellen die eiwitten maken?
- Waarom moet verbranding in cellen meerdere stappen plaatsvinden?
- Beschrijf de algemene functie van kern?
- Waarom is water naar levende organismen?
- Waarom bevatten bacteriën van nature restrictie -enzymen?
- Wat omdat mensen hun eigen voedsel niet kunnen produceren en moeten eten welk organisme zijn ze?
- Metalen vijfledige ring verlegt de grenzen van aromaticiteit

- Chemici ontwikkelen nieuw materiaal waarmee slim glas in recordtijd van kleur kan veranderen

- Afval CO2 wordt omgezet in ingrediënten voor brandstof, plastic en zelfs voedsel

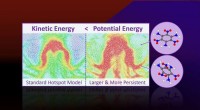
- Onderzoek onthult ontbrekende fysica in explosieve hotspots
- Het toevoegen van een inert polymeer aan plastic zonnecellen zorgt voor een hoog rendement en eenvoudige productie

 Hoe berekent u de versnelling?
Hoe berekent u de versnelling?  Het natuurlijke vermogen van hout gebruiken om te buigen tijdens het drogen om gebogen structuren te creëren
Het natuurlijke vermogen van hout gebruiken om te buigen tijdens het drogen om gebogen structuren te creëren Warmste mei ooit, Siberië 10C heter
Warmste mei ooit, Siberië 10C heter Welke snelheid reizen televisiegolven in de lucht?
Welke snelheid reizen televisiegolven in de lucht?  Freeze fighter:warmer wetsuit zal de duiktijd van de marine verlengen
Freeze fighter:warmer wetsuit zal de duiktijd van de marine verlengen Wat gebeurt er met zijn massa als het object een negatieve lading ontvangt?
Wat gebeurt er met zijn massa als het object een negatieve lading ontvangt?  In welk spectrale type zit uw zon?
In welk spectrale type zit uw zon?  Wat is de ionische lading voor H?
Wat is de ionische lading voor H?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

