
Wetenschap
Polaire moleculen en waterstofbruggen:de verbinding begrijpen
Polaire moleculen:
* Definitie: Een polair molecuul heeft een ongelijkmatige verdeling van elektronen, wat resulteert in een enigszins positief uiteinde (δ+) en een enigszins negatief uiteinde (δ-).
* Oorzaak: Deze ongelijke verdeling treedt op vanwege verschillen in elektronegativiteit (het vermogen van een atoom om elektronen aan te trekken) tussen de atomen in het molecuul.
* Voorbeeld: Water (H₂O) is een klassiek voorbeeld. Zuurstof is elektronegatiever dan waterstof, dus trekt het de elektronen naar zich toe, waardoor de zuurstofzijde enigszins negatief wordt en de waterstofzijde enigszins positief.
Waterstofbruggen:
* Definitie: Een waterstofbrug is een speciaal soort intermoleculaire kracht (tussen moleculen) die optreedt wanneer een waterstofatoom covalent gebonden is aan een zeer elektronegatief atoom (zoals zuurstof, stikstof of fluor) en ook wordt aangetrokken door het eenzame elektronenpaar op een ander elektronegatief atoom in een nabijgelegen molecuul.
* Vereiste: Waterstofbindingen kunnen zich alleen vormen tussen moleculen die polaire bindingen hebben, met name waarbij waterstof en een zeer elektronegatief atoom betrokken zijn.
* Kracht: Waterstofbindingen zijn relatief zwak vergeleken met covalente bindingen, maar ze zijn sterker dan andere intermoleculaire krachten.
De relatie:
Polaire moleculen zijn essentieel voor de vorming van waterstofbruggen. Dit is waarom:
* Attractie: Het enigszins positieve uiteinde van het ene polaire molecuul wordt aangetrokken door het enigszins negatieve uiteinde van een ander polair molecuul. Deze aantrekkingskracht is de basis van de waterstofbrug.
* Voorbeelden:
* Water: Watermoleculen vormen waterstofbruggen met elkaar, waardoor een sterk netwerk van intermoleculaire interacties ontstaat die verantwoordelijk zijn voor de unieke eigenschappen van water, zoals een hoog kookpunt en oppervlaktespanning.
* DNA: Waterstofbruggen houden de twee DNA-strengen bij elkaar en vormen de dubbele helixstructuur.
* Eiwitten: Waterstofbruggen zijn betrokken bij de vouwing en structuur van eiwitten, wat cruciaal is voor hun functie.
Samengevat: Polaire moleculen creëren de omstandigheden die nodig zijn voor de vorming van waterstofbruggen. De licht positieve en licht negatieve uiteinden van deze moleculen zorgen voor sterke interacties tussen moleculen, waardoor veel belangrijke chemische en biologische processen worden beïnvloed.
 Hoe het zeeleven reageert op verzuring van de oceaan
Hoe het zeeleven reageert op verzuring van de oceaan  pH-indicatoren begrijpen:hoe ze werken en kleurveranderingen
pH-indicatoren begrijpen:hoe ze werken en kleurveranderingen  Hoeveel molverhoudingen kunnen worden geschreven voor een chemische reactie met drie stoffen?
Hoeveel molverhoudingen kunnen worden geschreven voor een chemische reactie met drie stoffen?  Wat is een voorbeeld van een mechanisch mengsel of oplossing dat nog twee vaste stoffen bestond?
Wat is een voorbeeld van een mechanisch mengsel of oplossing dat nog twee vaste stoffen bestond?  Welke hydrochinon is een organische verbinding, het heeft een molaire massa van 110,1 gram boven mol en samenstelling 65,45 procent C 5,45 H 29,09 O per massa. de moleculaire formule?
Welke hydrochinon is een organische verbinding, het heeft een molaire massa van 110,1 gram boven mol en samenstelling 65,45 procent C 5,45 H 29,09 O per massa. de moleculaire formule?
 Wat zijn alle niet -levende dingen in een ecosysteem dat wordt genoemd?
Wat zijn alle niet -levende dingen in een ecosysteem dat wordt genoemd?  Toelaatbaar koolstofbudget hoogstwaarschijnlijk overschat
Toelaatbaar koolstofbudget hoogstwaarschijnlijk overschat Wat is een uniek kenmerk van het tropische regenwoud?
Wat is een uniek kenmerk van het tropische regenwoud?  Waarom bewegen stengel en wortel respectievelijk naar het lichte zwaartepunt van de aarde?
Waarom bewegen stengel en wortel respectievelijk naar het lichte zwaartepunt van de aarde?  Wat zijn twee andere namen voor een naaldbos?
Wat zijn twee andere namen voor een naaldbos?
Hoofdlijnen
- Slapende honden laten liggen? Nieuw onderzoek suggereert dat ze zelfs tijdens het snoozen vocalisaties kunnen verwerken
- Hoe wordt het verdelen van cellen in twee dochtercellen genoemd?
- Wat doet een kern in plantencel?
- Wat zijn pleiotrope eigenschappen?
- De volledige stadia van meiose:een gedetailleerd overzicht
- Genetische informatie opslaan is een belangrijke functie van?
- Hoe krijgt een organisme met één cel zuurstof en voedsel?
- Welke planten produceren naakte zaden?
- Wat zijn eencellige of eenvoudige meercellige eukaryotische organismen?
- Overtollige suiker helpt wittevlieg om de afweer van planten te ontgiften

- Meer dan H2O:technologie meet gelijktijdig 71 elementen in water, andere vloeistoffen

- Remedie tegen superbacteriën gevonden in kraaiheide

- Vormverschuivende protocellen duiden op de mechanica van het vroege leven

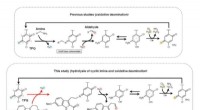
- Onderzoekers kijken naar de natuur om de geheimen van cyclische imine-splitsing te ontrafelen
 Gravity trekt gas en stof in een bol die dichtere heter wordende zonachtige ster wordt, begint zich te vormen?
Gravity trekt gas en stof in een bol die dichtere heter wordende zonachtige ster wordt, begint zich te vormen?  Als een diploïde organisme een genoom heeft dat uit tweeëntwintig chromosomen bestaat, hoeveel chromosomen zullen zijn gameten dan hebben?
Als een diploïde organisme een genoom heeft dat uit tweeëntwintig chromosomen bestaat, hoeveel chromosomen zullen zijn gameten dan hebben?  Airbus A380:van hightech wonder tot commerciële flop
Airbus A380:van hightech wonder tot commerciële flop Wat is het beste bewijs van crustal -verhoging?
Wat is het beste bewijs van crustal -verhoging?  Draagbare sensoren die gaslekken detecteren
Draagbare sensoren die gaslekken detecteren Wordt nantural gas veel gebruikt?
Wordt nantural gas veel gebruikt?  Een nieuwe manier om medicijnen af te leveren met nauwkeurige targeting
Een nieuwe manier om medicijnen af te leveren met nauwkeurige targeting Hoe vergelijkt een H R -diagram sterren?
Hoe vergelijkt een H R -diagram sterren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

