
Wetenschap
Propaanzuur versus ethanol:verschillen in zuurgraad begrijpen
* Structuur en hechting:
* Propaanzuur (CH3CH2COOH): De carboxylgroep (-COOH) heeft een polaire C=O-binding en een zeer polaire O-H-binding. Het zuurstofatoom in de -OH-groep is zeer elektronegatief, waardoor het H-atoom zuurder wordt. Het elektronenzuigende effect van de carbonylgroep verhoogt de zuurgraad verder.
* Ethanol (CH3CH2OH): De hydroxylgroep (-OH) in ethanol heeft ook een polaire OH-binding. De afwezigheid van de elektronenzuigende carbonylgroep maakt de O-H-binding echter minder polair en het H-atoom minder zuur.
* Stabiliteit van de geconjugeerde base:
* Propanoaation (CH3CH2COO-) :De negatieve lading op de geconjugeerde base wordt door resonantie gedelokaliseerd over twee zuurstofatomen, waardoor het anion wordt gestabiliseerd.
* Ethoxide-ion (CH3CH2O-) :De negatieve lading op het ethoxide-ion is gelokaliseerd op het zuurstofatoom, waardoor het minder stabiel is.
Samengevat: De aanwezigheid van de carbonylgroep in propaanzuur verhoogt de zuurgraad door de OH-binding polairder te maken en de geconjugeerde base te stabiliseren. Ethanol mist deze carbonylgroep, wat leidt tot een zwakkere zuurgraad.
 Hoe dood je onkruid rond bomen zonder de boom te kwetsen?
Hoe dood je onkruid rond bomen zonder de boom te kwetsen?  Welke voedingsstoffen krijgen organismen de neiging om van hun lokale ecosytem te komen?
Welke voedingsstoffen krijgen organismen de neiging om van hun lokale ecosytem te komen?  Feiten over de Catawba River Basin in North Carolina
Feiten over de Catawba River Basin in North Carolina  Actieve laag in verschillende vries-dooistadia wijzigt de dynamiek van de bodemademhaling
Actieve laag in verschillende vries-dooistadia wijzigt de dynamiek van de bodemademhaling Australië heeft heetste winter ooit
Australië heeft heetste winter ooit
Hoofdlijnen
- Wat zijn een ander orgaansysteem?
- Wat wordt er in een DNA -nucleotide gevonden?
- Noem 2 dingen die een plantcel een dier heeft, heeft niet?
- Nieuwe inzichten in hoe epilancine 15X bacteriën doodt
- mRNA: definitie, functie en structuur
- Soorten micro -organismen zijn te zien in een lichtmicroscoop?
- Waar produceert fotosynthese voedsel voor?
- Is een Sycamore -boom een angiosperm of gymnosperm?
- Wat is het verschil tussen bacteriën en levende organismen?
- Elektronenversnellers onthullen de radicale geheimen van antioxidanten

- Microscoop met elektroden wijst naar beter ontworpen apparaten die brandstof maken uit zonlicht

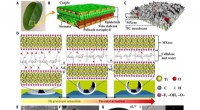
- Bio-geïnspireerde op MXene gebaseerde actuatoren voor programmeerbare slimme apparaten
- Micro-dispenser voor langdurige opslag en gecontroleerde afgifte van vloeistoffen

- 'S Werelds eerste ultrasone biosensor gemaakt in Australië
 Welk type vaste stof is minder dicht dan zijn vloeibare vorm?
Welk type vaste stof is minder dicht dan zijn vloeibare vorm?  Nieuw onderzoek geeft een betere kijk op de oceaanplaat onder Midden-Amerika
Nieuw onderzoek geeft een betere kijk op de oceaanplaat onder Midden-Amerika Het proces door welk gesmolten materiaal voegt nieuwe oceanische korst toe aan de oceaanbodem?
Het proces door welk gesmolten materiaal voegt nieuwe oceanische korst toe aan de oceaanbodem?  Waarom komen cellen voort uit eerder bestaande cellen?
Waarom komen cellen voort uit eerder bestaande cellen?  Wat zijn 3 metingen met verschillende eenheden die gelijk zijn aan 5 meter?
Wat zijn 3 metingen met verschillende eenheden die gelijk zijn aan 5 meter?  Wat is TRU Motion 200Hz?
Wat is TRU Motion 200Hz?  Hoe groot is een stellaire nevel?
Hoe groot is een stellaire nevel?  Hoe wordt elektriciteit gegenereerd?
Hoe wordt elektriciteit gegenereerd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

