
Wetenschap
De oplosmiddeleigenschappen van water:polariteit en oplossing begrijpen
Dit is waarom:
* Polariteit: Watermoleculen hebben een gebogen vorm, waarbij zuurstof licht negatief geladen is en waterstof licht positief geladen. Deze ongelijkmatige verdeling van de lading creëert een dipoolmoment, waardoor water een polair molecuul wordt.
* Attractie: De positieve uiteinden van watermoleculen worden aangetrokken door de negatieve uiteinden van andere polaire moleculen (zoals suikers, zouten en alcoholen), en omgekeerd. Deze aantrekkingskracht helpt de opgeloste moleculen uit elkaar te halen en op te lossen in water.
* Waterstofbinding: Watermoleculen kunnen waterstofbruggen vormen met elkaar en met andere polaire moleculen. Deze bindingen zijn sterk en helpen de opgeloste stoffen in oplossing te houden.
Daarentegen lossen niet-polaire moleculen (zoals oliën en vetten) niet gemakkelijk op in water, omdat ze niet de polaire aard hebben om met de watermoleculen te interageren.
 Welke producten worden gevormd op sterk verhitte ferrosulfaatkristallen?
Welke producten worden gevormd op sterk verhitte ferrosulfaatkristallen?  Opschalen naar nieuwe hoogten met gekko-geïnspireerde lijm
Opschalen naar nieuwe hoogten met gekko-geïnspireerde lijm Beschrijf wat er zou gebeuren als een positief geladen natriumatoom en negatief chloor in contact kwamen?
Beschrijf wat er zou gebeuren als een positief geladen natriumatoom en negatief chloor in contact kwamen?  Kan een verbinding in zijn samenstellende elementen worden gescheiden?
Kan een verbinding in zijn samenstellende elementen worden gescheiden?  Virusoppervlakken helpen ingenieurs bij het bestuderen van toepassingen voor vaccins en gentherapie
Virusoppervlakken helpen ingenieurs bij het bestuderen van toepassingen voor vaccins en gentherapie
Hoofdlijnen
- Wat zijn de organismen die meer nakomelingen produceren dan hun omgeving kan ondersteunen en ze met elkaar concurreren om te overleven?
- Wat draagt de eiercel bij aan een embryo?
- Dieren wiens basislichaamsplan kan worden omschreven als een buis erin zijn de?
- Wat vereist transcriptie in eukaryoten toevoeging aan RNA -polymerase?
- Hoe modificeren wetenschappers watermeloenen genetisch?
- Welke organellen moeten aanwezig zijn in een cel van geraniumblad voor ademhaling en fotosynthese?
- Wat kan polygene overerving verklaren?
- Welke soorten wormen leven in een savanne?
- Welk oceaandier heeft radiale lichaamssymmetrie?
- Lichte brandwonden met nieuwe zuren

- Operatie in een pil een mogelijke behandeling voor diabetes

- Biomining van de elementen van de toekomst

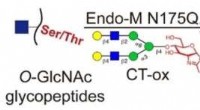
- Reversibele chemo-enzymatische labelstrategie maakt diepgaande analyse van eiwit O-GlcNAcylation mogelijk
- Chemputer belooft app-gestuurde revolutie voor medicijnproductie

 In welk gebied van wetenschap is het menselijk lichaam?
In welk gebied van wetenschap is het menselijk lichaam?  Begrijpt het Europese publiek de effecten van klimaatverandering op de oceaan?
Begrijpt het Europese publiek de effecten van klimaatverandering op de oceaan? Hoe wordt het genoemd als een stof die werd gevormd tijdens de reactie aan de rechterkant van de pijl in chemische reactie?
Hoe wordt het genoemd als een stof die werd gevormd tijdens de reactie aan de rechterkant van de pijl in chemische reactie?  Wat als we de oorlog zouden beëindigen?
Wat als we de oorlog zouden beëindigen?  Hoe het aantal elektronen te bepalen met Quantum Numbers
Hoe het aantal elektronen te bepalen met Quantum Numbers Nieuwe vingerafdrukken toegevoegd aan database voor chemische identificatie
Nieuwe vingerafdrukken toegevoegd aan database voor chemische identificatie Afbeelding:Grote Binoculaire Telescoop vangt eerste glimp op van NASA's OSIRIS-REx-ruimtevaartuig sinds lancering
Afbeelding:Grote Binoculaire Telescoop vangt eerste glimp op van NASA's OSIRIS-REx-ruimtevaartuig sinds lancering Waarom vliegt een satelliet niet uit de ruimte vanuit de sfeer?
Waarom vliegt een satelliet niet uit de ruimte vanuit de sfeer?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

