
Wetenschap
Elektronegativiteit in metalen:aantrekkingskracht en binding begrijpen
Dit is waarom:
* Metaalbinding: Metalen vormen bindingen waarbij elektronen worden gedelokaliseerd en over de hele structuur worden gedeeld, waardoor het minder waarschijnlijk is dat ze elektronen van andere atomen aantrekken.
* Elektropositieve aard: Metalen hebben de neiging elektronen te verliezen en positieve ionen te vormen, wat wijst op een lage aantrekkingskracht voor elektronen.
Hoewel sommige metalen een iets hogere elektronegativiteit hebben dan andere, zijn de meest elektronegatieve elementen niet-metalen , zoals fluor (F), zuurstof (O), chloor (Cl) en stikstof (N).
Samengevat: Er is geen 'meest elektronegatief metaal' omdat metalen over het algemeen elektropositief zijn en een lage elektronegativiteit hebben in vergelijking met niet-metalen.
 Oceaanplastic dat de kusten van Chili ooit verstikte, nu in hoeden van Patagonië
Oceaanplastic dat de kusten van Chili ooit verstikte, nu in hoeden van Patagonië  Conserverende landbouw leidt tot opmerkelijke verbetering van de gewasproductie en het levensonderhoud van boeren in Bangladesh
Conserverende landbouw leidt tot opmerkelijke verbetering van de gewasproductie en het levensonderhoud van boeren in Bangladesh Onderzoek toont drijvende factoren aan achter veranderingen tussen lokale en wereldwijde koolstofcycli
Onderzoek toont drijvende factoren aan achter veranderingen tussen lokale en wereldwijde koolstofcycli Waarom is het aardklimaat niet te warm noch koud?
Waarom is het aardklimaat niet te warm noch koud?  Nieuwe simulaties splitsen de potentiële impact van een grote aardbeving op per bouwlocatie en grootte
Nieuwe simulaties splitsen de potentiële impact van een grote aardbeving op per bouwlocatie en grootte
Hoofdlijnen
- Waarom moet het immuunsysteem pathogeen vernietigen?
- Noem drie manieren waarop bacteriën nuttig zijn?
- De fysieke kenmerken van een organisme worden het genoemd?
- Ik heb bloedgroep A en weet dat A op de een of andere manier anders is dan de andere typen, maar ik zou graag willen wat ze zijn.?
- Wat is de acrostic van microscoop?
- Wat is de inososfeer?
- Wat gebeurt er tijdens de G1-fase?
- Een cel verplaatst deeltjes van een gebied van mindere concentratie naar groter door wat?
- Genen dragen de informatie die bepaalt wat?
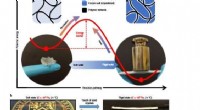
- Een hybride materiaal dat omkeerbaar schakelt tussen twee stabiele vaste toestanden
- Hoe technologie die is ontworpen voor de ruimte, kan helpen bij het opsporen van ziekten op planeet Aarde

- Gyroscoopmoleculen vormen kristal dat zowel solide als vol beweging is
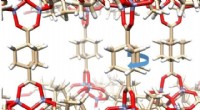
- Perovskietmaterialen:Neutronen tonen twinning in halide perovskieten

- Robuuste en goedkope katalysatoren voor waterstofproductie

 De geesteswetenschappen in Amerika – een bedreigde diersoort?
De geesteswetenschappen in Amerika – een bedreigde diersoort?  Uit onderzoek blijkt dat er een raciale ongelijkheid bestaat tussen wat zwarte en blanke leners betalen voor hypotheekleningen
Uit onderzoek blijkt dat er een raciale ongelijkheid bestaat tussen wat zwarte en blanke leners betalen voor hypotheekleningen  Lego-figuren maken geen kans tegen tijdomkering
Lego-figuren maken geen kans tegen tijdomkering Hoeveel energie zou je krijgen door een menselijk lichaam te verbranden?
Hoeveel energie zou je krijgen door een menselijk lichaam te verbranden?  Waarom hebben levende wezens en machines energie nodig?
Waarom hebben levende wezens en machines energie nodig?  Vragen over privacy bij het beoordelen van gebruikersaudio op Facebook
Vragen over privacy bij het beoordelen van gebruikersaudio op Facebook Grot van relikwieën gevonden onder Maya-ruïnes van Chichen Itza (update)
Grot van relikwieën gevonden onder Maya-ruïnes van Chichen Itza (update) Efficiëntie in fotokatalyse bleek plaatsgevoelig te zijn
Efficiëntie in fotokatalyse bleek plaatsgevoelig te zijn
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

