
Wetenschap
Stikstof versus arseen:onderzoek naar de belangrijkste verschillen en overeenkomsten
Stikstof (N)
* Niet-metaal: Het bestaat als gas bij kamertemperatuur en wordt aangetroffen in groep 15 van het periodiek systeem.
* Essentieel voor het leven: Het is een sleutelcomponent van eiwitten, nucleïnezuren (DNA en RNA) en de atmosfeer.
* Relatief niet-reactief: Het vormt stabiele moleculen zoals N₂ (stikstofgas) in de atmosfeer.
* Kan meerdere bindingen vormen: Stikstof kan drievoudige bindingen vormen, wat bijdraagt aan de stabiliteit ervan.
Arseen (As)
* Metalloïde: Het bevindt zich op de grens tussen metalen en niet-metalen en vertoont eigenschappen van beide. Het wordt gevonden in groep 15 van het periodiek systeem.
* Giftig: Arseen is een zeer giftig element.
* Reactiever dan stikstof: Het vormt gemakkelijk verbindingen met andere elementen.
* Kan in verschillende vormen bestaan: Het kan als vaste stof in verschillende allotropen (verschillende fysieke vormen) worden aangetroffen.
Overeenkomsten:
* Beide zitten in groep 15: Dit betekent dat ze hetzelfde aantal valentie-elektronen hebben (5).
* Beide kunnen covalente bindingen vormen: Ze delen elektronen met andere atomen om moleculen te vormen.
Verschillen:
* Chemische reactiviteit: Stikstof is relatief niet-reactief, terwijl arseen reactiever is.
* Toxiciteit: Stikstof is essentieel voor het leven, terwijl arseen zeer giftig is.
* Fysische toestand bij kamertemperatuur: Stikstof is een gas, terwijl arseen een vaste stof is.
Samenvattend:hoewel stikstof en arseen beide in dezelfde groep van het periodiek systeem zitten, worden hun overeenkomsten gecompenseerd door hun aanzienlijke verschillen in reactiviteit, toxiciteit en fysische eigenschappen.
 Wat de diepe bezuinigingen op onderzoek en ontwikkeling van DuPont betekenen voor de wetenschap
Wat de diepe bezuinigingen op onderzoek en ontwikkeling van DuPont betekenen voor de wetenschap  Ontdekking van een eenvoudig proces voor H2-productie met ammoniak als drager
Ontdekking van een eenvoudig proces voor H2-productie met ammoniak als drager Wat kan een vaste stof zijn als het niet koel en vloeistof is?
Wat kan een vaste stof zijn als het niet koel en vloeistof is?  Als de concentratie van één materiaal in een oplossing wordt gegeven, welke aanvullende informatie is nodig om een tweede oplossing te vinden?
Als de concentratie van één materiaal in een oplossing wordt gegeven, welke aanvullende informatie is nodig om een tweede oplossing te vinden?  Natriumchloride versus natriumjodide:een eenvoudige oplosbaarheidstest
Natriumchloride versus natriumjodide:een eenvoudige oplosbaarheidstest
 Wat is het verschil tussen aarde en omgeving?
Wat is het verschil tussen aarde en omgeving?  De verandering van de zeespiegel vanuit de ruimte in de gaten houden
De verandering van de zeespiegel vanuit de ruimte in de gaten houden Californiërs niet bereid om natuurbrandpreventie te subsidiëren
Californiërs niet bereid om natuurbrandpreventie te subsidiëren Diamantinsluitingen suggereren vrij stromend water op de grens tussen de bovenste en onderste mantel
Diamantinsluitingen suggereren vrij stromend water op de grens tussen de bovenste en onderste mantel Hoe bodemmicro-organismen uit de pas lopen door klimaatverandering
Hoe bodemmicro-organismen uit de pas lopen door klimaatverandering
Hoofdlijnen
- Wat zijn de 2 soorten DNA -plasmiden gevonden in micro -organismen?
- Bacteriën in de dikke darm zijn belangrijk omdat ze belangrijk synthetiseren?
- Onderzoek werpt licht op hoe conflicterende processen plaatsvinden binnen een enkele cel
- Van welke cellen wordt verwacht dat ze meer mitochondriën hebben?
- Wat zijn twee kenmerken van mRNA in eukaryoten?
- Wat is de grootste celstructuur?
- Wat is de toeschrijving van menselijke charectericstici aan oninbehoudobjecten?
- Alle volgende zijn belangrijke eigenschappen Prokaryoten behalve?
- Waarom is transcriptie belangrijk?
- Lab-on-a-disc-technologie belooft te versnellen, DNA-analyse ter plaatse vereenvoudigen

- Wetenschappers ontwikkelen een nieuwe methode om de efficiëntie van luchtreinigers te verbeteren

- Onderzoekers ontwikkelen een nieuw type synthetische moleculaire machine
- Lab-gekweekte pigmenten en voedselbijproducten:de toekomst van natuurlijke textielkleurstoffen

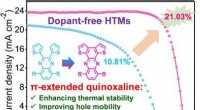
- Doteringsvrij, vochtstabiele organische lagen geven perovskiet-zonnecellen 21% efficiëntie
 Wat zijn feiten over kneedbare rotsen?
Wat zijn feiten over kneedbare rotsen?  Wat is het onderwerp in Song Black Hole Sun van Soundgarden?
Wat is het onderwerp in Song Black Hole Sun van Soundgarden?  Wat is de valentie van zwavel in MgSO4?
Wat is de valentie van zwavel in MgSO4?  Hoe testen wetenschappers hypothesen?
Hoe testen wetenschappers hypothesen?  Peking verlaat lijst van 200 meest vervuilde steden
Peking verlaat lijst van 200 meest vervuilde steden Hoe verkrijgen bacteriën de energie die ze nodig hebben?
Hoe verkrijgen bacteriën de energie die ze nodig hebben?  De kern van de aarde is verzonnen hoeveel lagen?
De kern van de aarde is verzonnen hoeveel lagen?  Onderzoekers onthullen verband tussen functietitels en gendergelijkheid
Onderzoekers onthullen verband tussen functietitels en gendergelijkheid
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

