
Wetenschap
Koolstofbinding:covalente obligaties en uitzonderingen begrijpen
Dit is waarom:
* Elektronenconfiguratie: Koolstof heeft 4 valentie-elektronen (elektronen in de buitenste schil). Om een stabiel octet (8 elektronen) te bereiken, moet het nog 4 elektronen winnen of delen.
* Covalente binding: Koolstof bereikt deze stabiliteit door zijn elektronen te delen met andere atomen via covalente bindingen. Elk gedeeld elektronenpaar telt mee voor het octet van beide atomen.
Uitzonderingen:
Hoewel koolstof gewoonlijk vier bindingen vormt, zijn er enkele uitzonderingen:
* Carbokationen: Dit zijn positief geladen koolstofionen die door het verlies van één elektron slechts drie bindingen vormen.
* Vrije radicalen: Koolstofatomen met een ongepaard elektron vormen ook slechts drie bindingen.
* Bepaalde ongebruikelijke moleculen: Bij sommige zeer reactieve of onstabiele moleculen kan koolstof met minder dan vier bindingen betrokken zijn, maar dit komt niet vaak voor.
Samengevat: Koolstof vormt gewoonlijk vier covalente bindingen, maar er zijn enkele specifieke omstandigheden waarin het er drie kan vormen.
 Welk metaal heeft de specifieke warmte van 0,30?
Welk metaal heeft de specifieke warmte van 0,30?  Wat zijn vier gebruik van metalen?
Wat zijn vier gebruik van metalen?  Wetenschappers identificeren schadelijke bacteriën op basis van hun DNA tegen zeer lage kosten
Wetenschappers identificeren schadelijke bacteriën op basis van hun DNA tegen zeer lage kosten Hoe kun je aniline en primair amine onderscheiden?
Hoe kun je aniline en primair amine onderscheiden?  Waarom is het symbool voor element zwavel anders dan de formule A -molecule zwavel?
Waarom is het symbool voor element zwavel anders dan de formule A -molecule zwavel?
 Marine krijgt concurrentievoordeel met onderzoek naar biologische oceaanzwermen
Marine krijgt concurrentievoordeel met onderzoek naar biologische oceaanzwermen Bahamas, Florida zet zich schrap als nieuwe orkaan Isaias neerstort
Bahamas, Florida zet zich schrap als nieuwe orkaan Isaias neerstort Wat is ecologische drift?
Wat is ecologische drift?  Uit nieuw onderzoek blijkt dat het zes weken lang meten van je voedselverspilling je gewoontes kan veranderen
Uit nieuw onderzoek blijkt dat het zes weken lang meten van je voedselverspilling je gewoontes kan veranderen  Hoe gaan mineralen en water een plant in?
Hoe gaan mineralen en water een plant in?
Hoofdlijnen
- Woestijnmieren kunnen de betrouwbaarheid van oriëntatiepunten beoordelen terwijl ze op zoek zijn naar de weg naar huis
- Wat is streptokokkengroep A?
- Alphabet passeert Apple als grootste bedrijf – wat nu?
- Welke groep levende wezens draagt het meest bij aan biogene sediment?
- Kun je me 5 voorbeelden van bacteriën geven?
- Welke organel is verantwoordelijk voor het synthetiseren van eiwitten?
- Hoe is een plantencel gespecialiseerd om zijn werk te doen?
- Wat is een evolutiepatroon waarin twee soorten de relatie tot elkaar evolueren?
- Amoeba-reproductie:van binaire splitsing tot genetische uitwisseling
- Alkaline versus niet-alkaline batterijen:belangrijkste verschillen uitgelegd

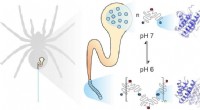
- Dynamiek van zijde-eiwitten is de sleutel tot uitstekende stabiliteit van spinzijde als biomateriaal
- Video:Waarom stinkende kazen stinken

- Hoe bacteriën edelmetalen kunnen terugwinnen uit batterijen van elektrische voertuigen

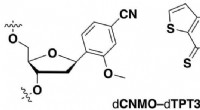
- Halfsynthetische bacteriën produceren onnatuurlijke eiwitten
 Wat voor soort boek kun je op fruit krijgen dat elektriciteit maakt?
Wat voor soort boek kun je op fruit krijgen dat elektriciteit maakt?  Hoe te schrijven in exponentiële vorm
Hoe te schrijven in exponentiële vorm Hoe dicht kun je de zon veilig benaderen voordat de intense hitte en straling fataal worden?
Hoe dicht kun je de zon veilig benaderen voordat de intense hitte en straling fataal worden?  Hoe beïnvloedt de hardheid van materialen snelheidsgeluid in vaste stoffen?
Hoe beïnvloedt de hardheid van materialen snelheidsgeluid in vaste stoffen?  Hier leest u hoe u ervoor kunt zorgen dat meer vrouwen topfuncties op universiteiten krijgen
Hier leest u hoe u ervoor kunt zorgen dat meer vrouwen topfuncties op universiteiten krijgen  Waarom zien we de spectaculaire gebeurtenissen in de lucht?
Waarom zien we de spectaculaire gebeurtenissen in de lucht?  Studie:Diepzeewezens die een feest of hongersnood leven vanwege energiestromen
Studie:Diepzeewezens die een feest of hongersnood leven vanwege energiestromen Welke term beschrijft opgeslagen energie?
Welke term beschrijft opgeslagen energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

