
Wetenschap
Niet-polaire covalente bindingen in zuurstof (O2) begrijpen
1. Gelijke elektronegativiteit: Beide zuurstofatomen in een O2-molecuul hebben dezelfde elektronegativiteit. Elektronegativiteit is het vermogen van een atoom om elektronen naar zich toe te trekken in een chemische binding. Omdat beide zuurstofatomen dezelfde elektronegativiteit hebben, delen ze de elektronen gelijk.
2. Symmetrische structuur: Het O2-molecuul heeft een symmetrische lineaire structuur, wat betekent dat de twee zuurstofatomen in een rechte lijn zijn gerangschikt. Deze symmetrische structuur zorgt er verder voor dat de elektronendichtheid gelijkelijk wordt verdeeld tussen de twee zuurstofatomen.
3. Geen dipoolmoment: Vanwege de gelijke elektronegativiteit en symmetrische structuur is er geen scheiding van lading binnen het O2-molecuul. Deze afwezigheid van ladingsscheiding betekent dat er geen dipoolmoment is, wat een maat is voor de polariteit van een molecuul.
Water (H2O) is daarentegen een polair molecuul omdat:
* Zuurstof is elektronegatiever dan waterstof.
* Het watermolecuul is gebogen, waardoor een ongelijkmatige verdeling van de elektronendichtheid ontstaat, met een gedeeltelijke negatieve lading op het zuurstofatoom en gedeeltelijke positieve lading op de waterstofatomen.
Daarom de gelijke elektronegativiteit en symmetrische structuur van het O2-molecuul zijn de belangrijkste redenen waarom het geen polaire covalente binding vormt.
 Waar is een samenvatting van de chemische geschiedeniskaars?
Waar is een samenvatting van de chemische geschiedeniskaars?  Chemici programmeren vloeibaar-kristallijne elastomeren om complexe draaibewegingen eenvoudig na te bootsen met behulp van licht
Chemici programmeren vloeibaar-kristallijne elastomeren om complexe draaibewegingen eenvoudig na te bootsen met behulp van licht Wat bevat een atoom?
Wat bevat een atoom?  Welk type verandering heeft invloed op de staatsmaterie maar geen chemische make -up?
Welk type verandering heeft invloed op de staatsmaterie maar geen chemische make -up?  Hoeveel totale zuurstofatomen 2CO2 en 3 H2O gecombineerd?
Hoeveel totale zuurstofatomen 2CO2 en 3 H2O gecombineerd?
 UAV-vliegtuigen bieden nieuwe inzichten in de vorming van de kleinste deeltjes in het noordpoolgebied
UAV-vliegtuigen bieden nieuwe inzichten in de vorming van de kleinste deeltjes in het noordpoolgebied Wat zijn de oplossingen voor druiven die door de klimaatverandering worden beïnvloed?
Wat zijn de oplossingen voor druiven die door de klimaatverandering worden beïnvloed?  Er is meer nodig dan goede bedoelingen om de afvalbergen van Nairobis op te ruimen
Er is meer nodig dan goede bedoelingen om de afvalbergen van Nairobis op te ruimen Hoe creëren de hersenen een ononderbroken kijk op de wereld?
Hoe creëren de hersenen een ononderbroken kijk op de wereld?  Snel, nauwkeurige schatting van het aardmagnetisch veld voor detectie van natuurrampen
Snel, nauwkeurige schatting van het aardmagnetisch veld voor detectie van natuurrampen
Hoofdlijnen
- Welk levensproces stelt organisme in staat om veranderingen in hun omgeving te reageren?
- Uit het Citizen Science-project blijkt dat respectvolle bootgebruikers worden beloond met magische ontmoetingen met dolfijnen
- Hoe homeostase de balans van uw lichaam handhaaft – de essentiële rol van thermoregulatie, pH, bloeddruk en hartslag
- Nieuwe bacteriesoort ontdekt in de darm
- Wat is het sterkste gen voor een eigenschap?
- Waarom is DNA -replicatie belangrijk voor de groei en ontwikkeling van een multi -cellulair organisme?
- Hoe wordt een eigenschap genoemd als het wordt bestuurd door meer dan één gen?
- Het belang van plantaardige cellen
- Evolutie begrijpen:het proces van verandering in organismen
- Palladiumkatalysator versnelt twee afzonderlijke reacties, bruikbare moleculen maken in één proces
- Onderzoekers ontwikkelen een koolstofveer met hoge samendrukbaarheid en rekbaarheid

- NIST gaat met de (slow) flow mee:nieuwe techniek kan biotech verbeteren, precisie geneeskunde

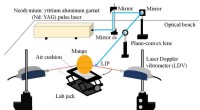
- De tijd is rijp! Een innovatieve contactloze methode voor het tijdig oogsten van zachtfruit
- Nieuwe materialen met een hoge zuurstof-ionengeleiding die een duurzame toekomst opent
 NASA- en NOAA-satellieten laten zien dat Erika Hispaniola beïnvloedt
NASA- en NOAA-satellieten laten zien dat Erika Hispaniola beïnvloedt  EU-leiders stellen besluit over klimaatdoelstelling voor 2050 uit
EU-leiders stellen besluit over klimaatdoelstelling voor 2050 uit Wat is een organisch sedimentair gesteente gevormd uit plantaardige materialen die voornamelijk werden gebruikt om elektriciteit te genereren?
Wat is een organisch sedimentair gesteente gevormd uit plantaardige materialen die voornamelijk werden gebruikt om elektriciteit te genereren?  Noem twee methoden met welke rotsen en mineralen uit de grond worden verwijderd?
Noem twee methoden met welke rotsen en mineralen uit de grond worden verwijderd?  Welke test kan worden gebruikt om de aanwezigheid van chloor te bevestigen?
Welke test kan worden gebruikt om de aanwezigheid van chloor te bevestigen?  Hoe een astrolabium te gebruiken:een praktische gids voor tijdwaarneming, navigatie en hemelobservaties
Hoe een astrolabium te gebruiken:een praktische gids voor tijdwaarneming, navigatie en hemelobservaties  Wat is 40 graden C in F?
Wat is 40 graden C in F?  NASA's OSIRIS-REx klaar voor landing op asteroïde Bennu
NASA's OSIRIS-REx klaar voor landing op asteroïde Bennu
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

