
Wetenschap
Hoge smelt- en kookpunten van ionische verbindingen begrijpen
1. Sterke elektrostatische krachten:
* Ionische bindingen: Ionische verbindingen worden gevormd door de overdracht van elektronen van een metaalatoom naar een niet-metaalatoom. Dit resulteert in de vorming van positief geladen kationen en negatief geladen anionen.
* Coulombische aantrekkingskracht: De tegengestelde ladingen van de ionen trekken elkaar aan met sterke elektrostatische krachten, waardoor een stijve roosterstructuur ontstaat. Deze krachten zijn aanzienlijk sterker dan de krachten tussen moleculen in covalente verbindingen.
2. Er is veel energie nodig om obligaties te verbreken:
* Smelten: Om een ionische verbinding te laten smelten, moet je voldoende energie leveren om de sterke elektrostatische krachten te overwinnen die de ionen in het rooster vasthouden. Dit vereist een grote hoeveelheid warmte, wat leidt tot een hoog smeltpunt.
* Koken: Koken kost zelfs meer energie dan smelten. Je moet voldoende energie leveren om de ionen volledig van elkaar te scheiden, waardoor de roosterstructuur volledig wordt verbroken. Dit vertaalt zich naar een hoog kookpunt.
3. Factoren die de smelt- en kookpunten beïnvloeden:
* Kosten: Hogere ladingen op de ionen leiden tot sterkere elektrostatische krachten en dus hogere smelt-/kookpunten. MgO heeft bijvoorbeeld een hoger smeltpunt dan NaCl omdat Mg²⁺ en O²⁻ hogere ladingen hebben dan Na⁺ en Cl⁻.
* Grootte: Kleinere ionen hebben een grotere elektrostatische aantrekkingskracht vanwege de kleinere afstand tussen hun centra. Dit resulteert ook in hogere smelt-/kookpunten.
Samengevat: De sterke elektrostatische krachten die de ionen bij elkaar houden in een ionenrooster vereisen een aanzienlijke hoeveelheid energie om te overwinnen, wat resulteert in de hoge smelt- en kookpunten die kenmerkend zijn voor ionische verbindingen.
Hoofdlijnen
- Welke DNA -mutaties zijn direct gekoppeld aan erfelijke ziekten?
- Hoe vormen wetenschappers kleinere groepen levende wezens?
- Welk deel van de cel neemt eiwitten en verandert ze zodat ze klaar zijn om de cel te verlaten?
- Wat is de functie van een gestreepte spiercel?
- Waarom zijn overervingspatronen bij mensen net zo gemakkelijk bestudeerde erwten of fruitvliegen?
- Hoe verhoudt Genesis zich tot de betekenis van gametogenese?
- Hoe schimmels eruit zien, hangt af van hoe zijn hyfen waar of onwaar zijn gerangschikt?
- Wat is geavanceerde menselijke genetica?
- Alternatief voor cellulaire ademhaling
De productie van energie uit organische verbindingen, zoals glucose, door oxidatie met behulp van chemische (meestal organische) verbindingen uit een cel als "elektronenacceptoren" wordt fermentatie genoemd. D
- Onderzoek naar het creëren van zelfreinigende oppervlakken via 3D-printen

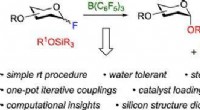
- Suikers synthetiseren:scheikundigen ontwikkelen methode om de opbouw van koolhydraten te vereenvoudigen
- Producten biologisch afbreekbaarder maken met zetmeel

- Kooldioxide binden met gebroken beton

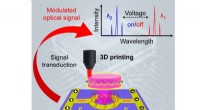
- Nieuw record:3D-geprinte optisch-elektronische integratie
 Is dit de definitie van breking- een golf buigen wanneer het door Earths Mediums gaat?
Is dit de definitie van breking- een golf buigen wanneer het door Earths Mediums gaat?  Waarom hangt de gezondheid van plant af van zijn cellen en weefsels?
Waarom hangt de gezondheid van plant af van zijn cellen en weefsels?  Waarom zien we verschillende sterrenbeelden in tijden van het jaar en in posities?
Waarom zien we verschillende sterrenbeelden in tijden van het jaar en in posities?  Brazilië:e-mail checken buiten kantooruren? Het is overwerk
Brazilië:e-mail checken buiten kantooruren? Het is overwerk  Space Facts voor Preschool
Space Facts voor Preschool  Wat is de afstand tussen Venus en Jupiter in ons zonnestelsel?
Wat is de afstand tussen Venus en Jupiter in ons zonnestelsel?  Wat is het proces door welke chemische energie van vrijgegeven voedselmoleculen?
Wat is het proces door welke chemische energie van vrijgegeven voedselmoleculen?  Handen in de sterren:de eerste internationale vergelijkende lijst van astronomische woorden in gebarentalen
Handen in de sterren:de eerste internationale vergelijkende lijst van astronomische woorden in gebarentalen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


