
Wetenschap
Natriumbicarbonaat en zoutzuurreactie:chemie uitgelegd
De reactie:
NaHCO₃ (aq) + HCl (aq) → NaCl (aq) + H₂O (l) + CO₂ (g)
Uitleg:
* Zuur-base-neutralisatie: Het zoutzuur (HCl) is een sterk zuur en natriumwaterstofcarbonaat (NaHCO₃) is een zwakke base. De reactie is in wezen een neutralisatiereactie waarbij het zuur en de base reageren om zout en water te vormen.
* Vorming van natriumchloride: Het natriumion (Na⁺) uit NaHCO₃ combineert met het chloride-ion (Cl⁻) uit HCl en vormt natriumchloride (NaCl), een keukenzout.
* Vorming van water: Het waterstofion (H⁺) uit HCl combineert met het waterstofcarbonaation (HCO₃⁻) uit NaHCO₃ en vormt koolzuur (H₂CO₃). Koolzuur is onstabiel en valt snel uiteen in water (H₂O) en kooldioxide (CO₂).
* Evolutie van kooldioxide: Er komt kooldioxidegas (CO₂) vrij, waardoor je bij deze reactie bruisen of borrelen waarneemt.
Opmerkingen:
* Bruisend: Het vrijkomen van kooldioxidegas veroorzaakt zichtbaar bruisen of borrelen in het reactiemengsel.
* Warmteproductie: De reactie is exotherm, wat betekent dat er warmte vrijkomt en dat de oplossing warm aanvoelt.
* Verandering in pH: De pH van de oplossing zal afnemen naarmate het zoutzuur wordt geneutraliseerd.
Gebruik:
Deze reactie heeft verschillende toepassingen:
* Antacidum: Natriumbicarbonaat wordt gebruikt in maagzuurremmers omdat het maagzuur (HCl) neutraliseert.
* Bakken: De reactie is verantwoordelijk voor de opkomst van brood en ander gebak.
* Chemische synthese: De reactie wordt gebruikt bij de chemische synthese om natriumchloride en andere verbindingen te produceren.
Veiligheid:
Zoutzuur is een bijtende stof, dus het is belangrijk om er voorzichtig mee om te gaan. Draag altijd de juiste veiligheidsuitrusting en werk in een goed geventileerde ruimte.
 Welke waterbron bevat meer anorganisch materiaaloppervlak of grondwater?
Welke waterbron bevat meer anorganisch materiaaloppervlak of grondwater?  Ongebruikelijke nanodeeltjes kunnen de zoektocht naar een kwantumcomputer ten goede komen
Ongebruikelijke nanodeeltjes kunnen de zoektocht naar een kwantumcomputer ten goede komen Is loodsulfaat een element of verbinding?
Is loodsulfaat een element of verbinding?  Datieve epitaxie:een nieuwe manier om kristalfilms te stapelen
Datieve epitaxie:een nieuwe manier om kristalfilms te stapelen Hoe de pH van ammoniakwater te berekenen met KB
Hoe de pH van ammoniakwater te berekenen met KB
 Nieuw robotlaboratorium dat de toxiciteit van algenbloei in Lake Erie volgt
Nieuw robotlaboratorium dat de toxiciteit van algenbloei in Lake Erie volgt De diepste meren in de VS:van Crater Lake tot Lake Clark
De diepste meren in de VS:van Crater Lake tot Lake Clark  Kanarie in de mijnwaarschuwing na nieuwe ontdekking van de effecten van verontreinigende stoffen op de vruchtbaarheid
Kanarie in de mijnwaarschuwing na nieuwe ontdekking van de effecten van verontreinigende stoffen op de vruchtbaarheid Zeer bezorgd:wetenschappers maken zich zorgen omdat het Antarctische zee-ijs afneemt
Zeer bezorgd:wetenschappers maken zich zorgen omdat het Antarctische zee-ijs afneemt  Rising Rock:de aardkorst heeft zijn eigen getijden,
Rising Rock:de aardkorst heeft zijn eigen getijden,
Hoofdlijnen
- Microben die onafhankelijk leven maar samenwerken en voedingsstoffen delen hoe het wordt genoemd?
- Welke eigenschappen zijn kenmerkend voor zowel eencellige als meercellige organismen?
- Wat is een complex koolhyraat dat plantenstelen en wortels versterkt?
- Hoe naburige walvissen elkaars taal leren
- Elektronenmicroscoopbeelden laten zien hoe cellen een vitaal mineraal opnemen
- Wat maakt deel uit van macro-evolutie?
- Welke planten hebben noten of kegels voor zaden?
- Voordelen van weefselcultuur samengesteld aan andere methoden aseksuele voortplanting?
- Evolueren organismen langzaam in de loop van de tijd en kunnen twee verschillende een gemeenschappelijke voorouder hebben?
- Biobased producten kunnen lichtgevend textiel produceren

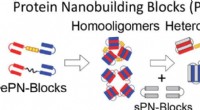
- Wetenschappers ontwikkelen eiwitten die zichzelf assembleren tot supramoleculaire complexen
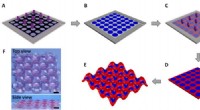
- Hydrogels met periodiek patroon:een model voor coöperatieve vervorming
- Door het kijkglas:ontrafelen hoe ionen bewegen in fosfaatglas

- Perfecte dranken en vloeibare voeding tot op moleculair niveau

 Hoe een 3D-model van het ademhalingssysteem te maken
Hoe een 3D-model van het ademhalingssysteem te maken Waarom het brandseizoen van 2020 zo hels was
Waarom het brandseizoen van 2020 zo hels was  Is de maan enige planeet waar mensen zijn geweest?
Is de maan enige planeet waar mensen zijn geweest?  Welke kleuren meng je om neongeel te maken?
Welke kleuren meng je om neongeel te maken?  Welke organismen zijn autotrofe?
Welke organismen zijn autotrofe?  Nieuwe tool voor fotovoltaïsche zonne-energie berekent nauwkeurig degradatiesnelheden, geld besparen en zakelijke beslissingen begeleiden
Nieuwe tool voor fotovoltaïsche zonne-energie berekent nauwkeurig degradatiesnelheden, geld besparen en zakelijke beslissingen begeleiden Welke naam van de wetenschapper die de aarde ontdekt?
Welke naam van de wetenschapper die de aarde ontdekt?  Wat gebeurt er met een ster wanneer de waterstof helium wordt?
Wat gebeurt er met een ster wanneer de waterstof helium wordt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

