
Wetenschap
Basisdissociatieconstante (Kb) en evenwicht begrijpen
De reactie:
```
B + H₂O ⇌ BH⁺ + OH⁻
```
Basisdissociatieconstante (Kb):
Kb is de evenwichtsconstante voor de reactie van een zwakke base (B) met water. Het meet de mate waarin de base in water dissocieert en zijn geconjugeerde zuur (BH⁺) en hydroxide-ionen (OH⁻) vormt.
Formule voor Kb:
```
Kb =[BH⁺] [OH⁻] / [B]
```
Waar:
* [BH⁺] is de evenwichtsconcentratie van het geconjugeerde zuur.
* [OH⁻] is de evenwichtsconcentratie van hydroxide-ionen.
* [B] is de evenwichtsconcentratie van de zwakke base.
Kb begrijpen:
* Een grotere Kb-waarde duidt op een sterkere base. Dit betekent dat de base gemakkelijker dissocieert in water, waardoor een hogere concentratie OH⁻-ionen ontstaat.
* Een kleinere Kb-waarde duidt op een zwakkere base. Dit betekent dat de base minder gemakkelijk dissocieert, wat resulteert in een lagere concentratie OH⁻-ionen.
Voorbeeld:
Als je een oplossing hebt van een zwakke base met een Kb van 1,0 x 10⁻⁵, betekent dit dat de base relatief zwak is. Slechts een klein deel van de basismoleculen zal in water dissociëren en de geconjugeerde zuur- en hydroxide-ionen vormen.
 Chemische synthese met behulp van titaniumdioxide:een milieuvriendelijke en innovatieve aanpak
Chemische synthese met behulp van titaniumdioxide:een milieuvriendelijke en innovatieve aanpak  Gebruik van zonlicht om de toekomst te voeden via covalente organische raamwerken
Gebruik van zonlicht om de toekomst te voeden via covalente organische raamwerken Als je krijt met water mengt en vervolgens verdampt, wat heb je dan?
Als je krijt met water mengt en vervolgens verdampt, wat heb je dan?  Thermosflessen:de wetenschap van isolatie begrijpen
Thermosflessen:de wetenschap van isolatie begrijpen  Biologisch afbreekbare gewasbeschermingsmiddelen zonder risico's of bijwerkingen
Biologisch afbreekbare gewasbeschermingsmiddelen zonder risico's of bijwerkingen
 De kern en de mantel van de aarde zijn op een wanordelijke manier gescheiden
De kern en de mantel van de aarde zijn op een wanordelijke manier gescheiden Wat is de beschermende stof die het waterverlies uit een blad beperkt?
Wat is de beschermende stof die het waterverlies uit een blad beperkt?  Nieuwe studie maakt regionale voorspelling van uranium in grondwater mogelijk
Nieuwe studie maakt regionale voorspelling van uranium in grondwater mogelijk Kolenstof en smogplaag leeft op Zuid-Afrika Highveld
Kolenstof en smogplaag leeft op Zuid-Afrika Highveld Duurzaamheid van het voedselsysteem vereist een lager energieverbruik
Duurzaamheid van het voedselsysteem vereist een lager energieverbruik
Hoofdlijnen
- Wat voor soort schimmels reproduceert niet seksueel?
- Onderzoekers ontdekken dat calcium aardappelplanten kan beschermen tegen bacteriële verwelking
- Massa-extincties verwijderen soorten, maar geen ecologische variëteit
- Oplossen van hoe een complexe ziekte eiken bedreigt
- Wat zijn theorieën over hoe mensen zijn gemaakt?
- Sommige bedreigde diersoorten kunnen niet langer in het wild overleven. Moeten we dus hun genen veranderen?
- Welke celfunctie heeft het nucleïnezuur?
- Wat is de rol van Cloropyll in de cel?
- Nieuwe bevindingen werpen licht op hoe bella-motten gif gebruiken om partners aan te trekken
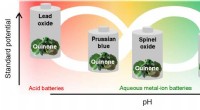
- Goedkoop organisch materiaal geeft veilige batterijen een langere levensduur
- Plantaardige alkaloïden beschermen rijst, kiwi en citrus van schadelijke bacteriën

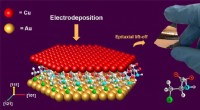
- Onderzoekers gebruiken aminozuren om hoogwaardige dunne koperfilms te laten groeien
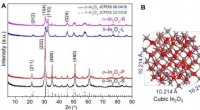
- Efficiënte indiumoxidekatalysatoren ontworpen voor CO2-hydrogenering tot methanol
- Nieuwe methode om composieten te maken met vormgeheugen

 Hoe oud is de vulkaan Soufriere Hills?
Hoe oud is de vulkaan Soufriere Hills?  Garnalenvisserij in New England voor minstens een jaar gesloten
Garnalenvisserij in New England voor minstens een jaar gesloten Hoe worden de landlucht en het water elke dag verwarmd?
Hoe worden de landlucht en het water elke dag verwarmd?  Welke organellen kunnen de krachtpatsers van cel worden genoemd?
Welke organellen kunnen de krachtpatsers van cel worden genoemd?  Hoeveel 20c -munten passen in een liter?
Hoeveel 20c -munten passen in een liter?  Hoe Caterpillar graaf-laadcombinaties werken
Hoe Caterpillar graaf-laadcombinaties werken  Wat maken kristallen en kokend water?
Wat maken kristallen en kokend water?  Egyptische rechtbank oordeelt over Uber, Careem illegaal; hoger beroep verwacht
Egyptische rechtbank oordeelt over Uber, Careem illegaal; hoger beroep verwacht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

