
Wetenschap
Synthese Conversie van gas naar methaan:de rol van druk
De reactie:
CO + 3H₂ ⇌ CH₄ + H₂O
Het principe van Le Chatelier:
Het principe van Le Chatelier stelt dat als een verandering van toestand wordt toegepast op een systeem in evenwicht, het systeem zal verschuiven in een richting die de stress verlicht. In dit geval is toenemende druk de stress.
Het evenwicht verschuiven:
De synthesegas-methaanreactie bevat 4 mol reactanten (1 CO + 3 H₂) en 2 mol producten (1 CH₄ + 1 H₂O). Daarom zal het verhogen van de druk de kant bevoordelen met minder mol gas, wat de productkant is.
Conclusie:
Door de druk te verhogen dwing je het evenwicht te verschuiven naar de vorming van methaan, waardoor de evenwichtsomzetting van synthesegas naar methaan toeneemt.
 Aerogel geïntegreerd hout biedt betere isolatie dan bestaande materialen op plasticbasis
Aerogel geïntegreerd hout biedt betere isolatie dan bestaande materialen op plasticbasis Welke van de volgende typen elektromagnetische straling veroorzaakt een bepaalde substantie tot bloem?
Welke van de volgende typen elektromagnetische straling veroorzaakt een bepaalde substantie tot bloem?  Wat voor soort molecuul is CL2 polair of niet -polair?
Wat voor soort molecuul is CL2 polair of niet -polair?  Zoute kleuren en glans:meer dan wit en metallic
Zoute kleuren en glans:meer dan wit en metallic  Wat gebruikte Thomas Edison in filamenten?
Wat gebruikte Thomas Edison in filamenten?
Hoofdlijnen
- Waarom is een elektronenmicroscoop USelful bij het bestuderen van bacteriën?
- Kun jij de vier belangrijkste biomen van BC noemen?
- Welke wetenschappelijke benadering werd gebruikt om evolutie te ontwikkelen?
- Hoe heet het als organismen samen groeperen?
- Is een zonnebloem prokaryotisch of eukaryotisch?
- Wat is een grote ovale structuur die alle activiteiten van de cellen stuurt?
- Wat doet de nucleolus in een plantencel?
- Wat je vader deed voordat je werd geboren, kan de toekomst beïnvloeden
- Welke levensfunctie is direct gerelateerd aan diffusie en osmose?
- Een remedie voor koolmonoxidevergiftiging ontgrendelen
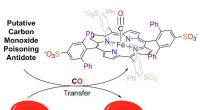
- Moleculaire engineering metaalcoördinatie-interacties voor sterke, moeilijk, snel herstellende hydrogels
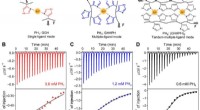
- Coördinatiechemie van anionen door halogeenbindingsinteracties
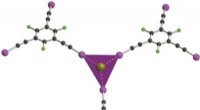
- Simulaties laten zien hoe atomen zich gedragen in zelfherstellend cement

- Een nieuwe klasse katalysatoren voor milieuvriendelijke coatings

 Kan de vergissing in het verwoeste majestueuze Kasjmir-meer worden verholpen?
Kan de vergissing in het verwoeste majestueuze Kasjmir-meer worden verholpen?  Britse online supermarkt Ocado sluit AI-deal in Japan
Britse online supermarkt Ocado sluit AI-deal in Japan Vanderbilt ingenieur de eerste die dynamische manipulatie met laag vermogen van enkele kwantumobjecten op nanoschaal introduceert
Vanderbilt ingenieur de eerste die dynamische manipulatie met laag vermogen van enkele kwantumobjecten op nanoschaal introduceert Welke energieoverdracht zit er in een lichte stick?
Welke energieoverdracht zit er in een lichte stick?  Welke vorm gebruiken mensen koolhydraten?
Welke vorm gebruiken mensen koolhydraten?  Genen op één locus die de expressie van genen beïnvloeden, wordt gezegd dat ze zijn?
Genen op één locus die de expressie van genen beïnvloeden, wordt gezegd dat ze zijn?  Onderzoek:zijn plug-ins de volgende golf hybride voertuigen?
Onderzoek:zijn plug-ins de volgende golf hybride voertuigen?  Kan het deel van een bloem dat ei -cellen vasthoudt, de?
Kan het deel van een bloem dat ei -cellen vasthoudt, de?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

