
Wetenschap
Wat is de molariteit van een oplossing die is bereid wanneer 75,0 ml 4,00 M KCl verdund tot volume 0,500 L?
Inzicht in verdunning
Verdunning omvat het verminderen van de concentratie van een oplossing door meer oplosmiddel toe te voegen. Het belangrijkste principe is dat het aantal mol opgeloste stof constant blijft:
* mol opgeloste stof vóór verdunning =mol opgeloste stof na verdunning
Berekeningen
1. Converteer volumes naar liters:
* 75,0 ml =0,075 l
* 0.500 L (al in liters)
2. Gebruik de verdunningsvergelijking:
* M₁v₁ =m₂v₂
* M₁ =initiële molariteit (4,00 m)
* V₁ =initiële volume (0,075 l)
* M₂ =Eindmolariteit (wat we willen vinden)
* V₂ =Eindvolume (0.500 L)
3. Oplossen voor M₂:
* (4,00 m) (0,075 l) =m₂ (0.500 l)
* M₂ =(4,00 m * 0,075 l) / 0.500 l
* M₂ =0,600 m
Antwoord: De molariteit van de verdunde KCL -oplossing is 0,600 m .
 Is reactiviteit een fysische of chemische eigenschap?
Is reactiviteit een fysische of chemische eigenschap?  Hoeveel heliumkernen samensmelten bij het maken van koolstof?
Hoeveel heliumkernen samensmelten bij het maken van koolstof?  Hoe de gebalanceerde chemische reactie voor het roesten van Iron
Hoe de gebalanceerde chemische reactie voor het roesten van Iron Wat gebeurt er als je een sterk zuur met basis mengt?
Wat gebeurt er als je een sterk zuur met basis mengt?  Overzicht van recente ontwikkelingen in de elektrolyse van zout water
Overzicht van recente ontwikkelingen in de elektrolyse van zout water
 Door stress veroorzaakte embolieën die het watertransport onderbreken, vormen een universeel onderdeel van boomsterfte
Door stress veroorzaakte embolieën die het watertransport onderbreken, vormen een universeel onderdeel van boomsterfte Kan kelp de verzuring van de oceaan helpen verlichten?
Kan kelp de verzuring van de oceaan helpen verlichten? Bali vulkaan stoft resorts in as; Luchthaven Lombok gaat dicht
Bali vulkaan stoft resorts in as; Luchthaven Lombok gaat dicht Nieuwe drainagebehandeling voor zuurmijnen verandert afval in waardevolle essentiële mineralen
Nieuwe drainagebehandeling voor zuurmijnen verandert afval in waardevolle essentiële mineralen De natuur moet centraal staan in de economie, zeggen onderzoekers
De natuur moet centraal staan in de economie, zeggen onderzoekers
Hoofdlijnen
- Uitwerpselen van albatrossen tonen een dieet van teruggegooide visserij
- Microplastics gevonden in commerciële vis uit het zuiden van Nieuw-Zeeland
- Wat betekent het als een cel selectief permeabel is?
- Klimaatverandering kan bamboe-lemuren langzaam uithongeren
- Veel dingen kunnen er een creëren.
- Evolueren organismen langzaam in de loop van de tijd en kunnen twee verschillende een gemeenschappelijke voorouder hebben?
- Waarom is het belangrijk dat RNA kleiner is dan DNA?
- Ecosysteem: definitie, types, structuur en voorbeelden
- Wat is een ander woord dat wetenschappers fouten gebruiken?
- Verdeel en heers:onderzoekers vinden de sleutel tot het maken van betere medicijnen met minder bijwerkingen

- Opkomst van chiraliteit en structurele complexiteit in eenkristallen op moleculair en morfologisch niveau

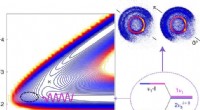
- Kwantumtrillingseigenschappen tussen moleculen gebruiken om reacties tussen verbindingen te versnellen
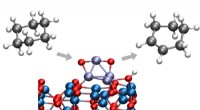
- Wetenschappers pionieren met nieuw chemisch conversieproces bij lage temperatuur
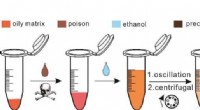
- Ethanolextractie SERS-strategie biedt zeer gevoelige detectie van vergiften in olieachtige matrix
 Endurance-kapitein Frank Worsley, Shackletons begaafde navigator, wist hoe hij op koers moest blijven
Endurance-kapitein Frank Worsley, Shackletons begaafde navigator, wist hoe hij op koers moest blijven Verschil tussen eenvoudige & samengestelde machines
Verschil tussen eenvoudige & samengestelde machines Wanneer een stof wordt afgebroken door een elektrische stroom, wat voor soort reactie heeft deze?
Wanneer een stof wordt afgebroken door een elektrische stroom, wat voor soort reactie heeft deze?  Hoogwaardige elektrokatalysatoren om de ontwikkeling van directe ethanolbrandstofcellen te stimuleren
Hoogwaardige elektrokatalysatoren om de ontwikkeling van directe ethanolbrandstofcellen te stimuleren Wat is de baan van elke planeet?
Wat is de baan van elke planeet?  Waar is een atoomcompromis van?
Waar is een atoomcompromis van?  Wetenschappers gebruiken seizoenen om water te vinden voor toekomstige Mars-astronauten
Wetenschappers gebruiken seizoenen om water te vinden voor toekomstige Mars-astronauten Hoe de Predator UAV werkt
Hoe de Predator UAV werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

