
Wetenschap
Metaal versus ionische roostersterkte:een gedetailleerde vergelijking
* Metaalbinding: Metalen hebben een uniek type binding dat metallische binding wordt genoemd. Bij dit type binding worden de valentie-elektronen gedelokaliseerd, wat betekent dat ze vrij door het hele rooster kunnen bewegen. Hierdoor ontstaat een sterke ‘zee van elektronen’ die de metaalatomen bij elkaar houdt.
* Ionische binding: Ionische verbindingen worden bij elkaar gehouden door elektrostatische aantrekking tussen tegengesteld geladen ionen. Hoewel deze aantrekkingskracht sterk is, is deze niet zo sterk als de gedelokaliseerde elektronenlijm in metalen.
Hier is een overzicht van de verschillen in roosterstructuur:
Metalen:
* Sterk: De gedelokaliseerde elektronen maken metaalbindingen extreem sterk.
* Nodulair en kneedbaar: De ‘zee van elektronen’ zorgt ervoor dat de atomen langs elkaar kunnen glijden zonder de bindingen te verbreken, waardoor metalen buigzaam en werkbaar worden.
* Goede geleiders van warmte en elektriciteit: De vrij bewegende elektronen kunnen gemakkelijk warmte en elektriciteit transporteren.
Ionische verbindingen:
* Broos: De stijve structuur van ionische verbindingen zorgt ervoor dat ze gemakkelijk versplinteren als er kracht op wordt uitgeoefend.
* Hoge smelt- en kookpunten: De sterke elektrostatische krachten vereisen veel energie om te breken.
* Goede geleiders van elektriciteit in de gesmolten staat: De ionen kunnen vrij bewegen wanneer de verbinding wordt gesmolten, waardoor elektriciteit kan stromen.
Samengevat: De sterke, gedelokaliseerde elektronenbindingen in metalen maken hun roosters veel sterker dan die in ionische verbindingen.
 Welk element heeft 6 valentie -elektronen en 52 protonen in de kern?
Welk element heeft 6 valentie -elektronen en 52 protonen in de kern?  Heeft baksteen een duidelijke chemische samenstelling?
Heeft baksteen een duidelijke chemische samenstelling?  3 voorbeelden van organische Ang Anorganic?
3 voorbeelden van organische Ang Anorganic?  Gebruikt als een legering in ballenpuntpennen Bijna tweemaal dichte lood De sterke geur die door dit metaal wordt gegeven, is het resultaat van zijn zeer giftige oxide?
Gebruikt als een legering in ballenpuntpennen Bijna tweemaal dichte lood De sterke geur die door dit metaal wordt gegeven, is het resultaat van zijn zeer giftige oxide?  Chemische formule voor koper 1 oxide?
Chemische formule voor koper 1 oxide?
 Pijpleidingbedrijf bereikt voorlopige schikking in rechtszaken over olieramp in Californië
Pijpleidingbedrijf bereikt voorlopige schikking in rechtszaken over olieramp in Californië Sterkste aardbeving sinds vulkaanuitbarsting doet Spaans eiland schudden
Sterkste aardbeving sinds vulkaanuitbarsting doet Spaans eiland schudden Industriële chemicaliën gaan tijdens de zwangerschap van moeder op foetus
Industriële chemicaliën gaan tijdens de zwangerschap van moeder op foetus Veranderingen in neerslagpatronen beïnvloeden natuurlijke selectie op wereldschaal
Veranderingen in neerslagpatronen beïnvloeden natuurlijke selectie op wereldschaal Waarom natuurbrandrook vooral slecht is voor je gezondheid
Waarom natuurbrandrook vooral slecht is voor je gezondheid
Hoofdlijnen
- Wat zijn de drie wortels van de evolutie van de wetenschap?
- Wetenschapper die bijdragen aan uw kennis over cel?
- Wat is een reactie op stimuli of omgeving die wordt genoemd?
- Is cytoplasma in een plant en dier?
- Gerelateerde organismen worden minder hetzelfde door de convergente evolutie of uiteenlopende evolutie van preditatie aanpassing?
- Hoe een haai te volgen:nieuw onderzoek onthult waar, waarom en hoe haaien en wildvissen elkaar overlappen
- Is er maar één wetenschappelijke methode.
- Wat doen bioligiest?
- Enzymcomplexen die eiwitten afbreken heten?
- Moleculen net zo gemakkelijk vastbinden als veters

- Een vreemd fenomeen ontrafelen dat zowel de prestaties van lithium-ionbatterijen helpt als schaadt

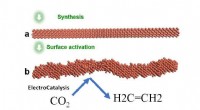
- Onderzoekers ontdekken effectieve manier om koolstofdioxide om te zetten in ethyleen
- Onderzoekers ontwikkelen sensoren die menselijke biomarkers en giftig gas detecteren
- Fosforescerend materiaal geïnspireerd op glow in the dark hout

 Welke geweldige dingen vertegenwoordigen sterren in de lucht?
Welke geweldige dingen vertegenwoordigen sterren in de lucht?  Hoe voldoet de DNA -structuur aan de vereisten van een erfelijk molecuul?
Hoe voldoet de DNA -structuur aan de vereisten van een erfelijk molecuul?  Wat is de juiste term voor een verschrompelde dierencel?
Wat is de juiste term voor een verschrompelde dierencel?  Welke term beschrijft de koeling van een gas door uitbreiding?
Welke term beschrijft de koeling van een gas door uitbreiding?  Hoe een Engineering Ruler
Hoe een Engineering Ruler Welke plaats zou Lunar Landscape hebben?
Welke plaats zou Lunar Landscape hebben?  Onderzoek naar het terugkeerbeleid van bedrijven biedt richtlijnen voor prijsstelling, geeft terug, terugbetalingen
Onderzoek naar het terugkeerbeleid van bedrijven biedt richtlijnen voor prijsstelling, geeft terug, terugbetalingen Journal Nature trekt onderzoek naar opwarming van de oceaan in
Journal Nature trekt onderzoek naar opwarming van de oceaan in
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

