
Wetenschap
Wat gebeurt er met de temperatuur van naftaleen tijdens het smelten?
Dit is waarom:
* smelten is een faseverandering: De energie die aan het naftaleen wordt toegevoegd, wordt gebruikt om de bindingen tussen de moleculen in de vaste toestand te verbreken, waardoor ze vrijer kunnen bewegen en overstappen naar de vloeibare toestand.
* constante temperatuur tijdens faseverandering: Deze energie -input verhoogt niet de kinetische energie van de moleculen, die direct gerelateerd is aan de temperatuur. In plaats daarvan wordt het gebruikt om de intermoleculaire krachten te overwinnen die de vaste structuur bij elkaar houden.
Daarom, hoewel je warmte toevoegt, blijft de temperatuur op het smeltpunt (ongeveer 80,2 ° C voor naftaleen) totdat alle vaste stof is gesmolten.
 Welke problemen worden veroorzaakt door zwaveldioxide?
Welke problemen worden veroorzaakt door zwaveldioxide?  Wat is de chemische reactie van het metabolisme vereist?
Wat is de chemische reactie van het metabolisme vereist?  Wat is het product wanneer zink en zilvernitraat een enkele vervangende reactie ondergaan?
Wat is het product wanneer zink en zilvernitraat een enkele vervangende reactie ondergaan?  Hoe verschillen de reactanten van fotosynthese van chemosynthese?
Hoe verschillen de reactanten van fotosynthese van chemosynthese?  Wat zijn de producten van pyruvaatoxidatie?
Wat zijn de producten van pyruvaatoxidatie?
Hoofdlijnen
- Wat zijn twee van de dingen die bacteriën nodig hebben om te vermenigvuldigen?
- Wat is plaveiselepitheelcellen en trichomonas of spermatozoa?
- Wat maakt avocado’s eigenlijk slecht voor het milieu?
- Is het vasculaire weefsel dat water en voedingsstoffen in een plant phoem leidt?
- Twee soorten fagocyten
- Fossielen van zaagvissen suggereren dat tanden waarschijnlijk zijn geëvolueerd uit schubben in oude vissen
- Waarom gebruiken cellen GTP in plaats van ATP bij celsignalering?
- Chromosomen wisselen genetische informatie uit via het proces waarvan?
- Is transporteiwit vereist voor niet -polaire moleculen?
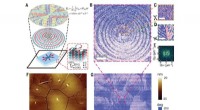
- Concentrische cirkelvormige polarisatiebanden gevonden in een ferro-elektrisch polymeer
- Druk kan de sleutel zijn tot het bestrijden van klimaatverandering met thermo-elektrische generatoren

- Geavanceerde polymeren helpen de waterzuivering te stroomlijnen, milieusanering

- Wetenschappers bereiken directe elektrokatalytische reductie van koolstofdioxide, wekt hoop op slimme koolstofafvang

- Afstembare omgekeerde fotochromen in vaste toestand

 Waarom de zon in een binair systeem?
Waarom de zon in een binair systeem?  Wat kun je aannemen als een elektron naar een hoger energieniveau gaat?
Wat kun je aannemen als een elektron naar een hoger energieniveau gaat?  Verklaar het verschil uit tussen feiten van wetenschap en wet op de wet?
Verklaar het verschil uit tussen feiten van wetenschap en wet op de wet?  Bijna 90 procent van de All-Stars is op welk moment in hun levenscycli?
Bijna 90 procent van de All-Stars is op welk moment in hun levenscycli?  Deeltjesfysici ontdekken een mysterieuze structuur in de Grote Piramide – zo deden ze dat
Deeltjesfysici ontdekken een mysterieuze structuur in de Grote Piramide – zo deden ze dat  Welk groot object heeft een korstkern en mantel?
Welk groot object heeft een korstkern en mantel?  Wat zijn de lagen van Jupiter?
Wat zijn de lagen van Jupiter?  Wat zijn enkele bronnen van licht die warmte produceren?
Wat zijn enkele bronnen van licht die warmte produceren?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

