
Wetenschap
Expressie voor werk gedaan in het isotherm- en adiabatisch proces?
isotherme proces
* Definitie: Een isotherme proces treedt op bij constante temperatuur.
* werk gedaan: Het werk dat in een isotherme proces wordt uitgevoerd, wordt gegeven door:
`` `
W =nrt * ln (v₂/v₁)
`` `
waar:
* W is het werk gedaan
* n is het aantal mol gas
* R is de ideale gasconstante
* T is de constante temperatuur
* V₁ is het eerste volume
* V₂ is het laatste deel
* Verklaring: In een isotherme proces blijft de interne energie van het systeem constant (omdat de temperatuur constant is). Daarom wordt alle aan het systeem toegevoegde warmte gebruikt om te werken aan de omgeving. De natuurlijke logaritme -term weerspiegelt de uitbreiding of compressie van het gas.
adiabatisch proces
* Definitie: Een adiabatisch proces treedt op zonder warmte -uitwisseling tussen het systeem en zijn omgeving (q =0).
* werk gedaan: Het werk dat in een adiabatisch proces wordt uitgevoerd, wordt gegeven door:
`` `
W =(p₂v₂ - p₁v₁) / (1 - γ)
`` `
waar:
* W is het werk gedaan
* P₁ en V₁ zijn de begindruk en volume
* P₂ en V₂ zijn de uiteindelijke druk en volume
* γ is de adiabatische index (verhouding van specifieke heats, CP/CV)
* Verklaring: In een adiabatisch proces wordt het systeem geïsoleerd van zijn omgeving, dus het werk is volledig ten koste van de interne energie van het systeem. De adiabatische index γ vertegenwoordigt de relatie tussen warmtecapaciteit bij constante druk (CP) en constant volume (CV), die specifiek is voor het gas.
Sleutelpunten om te onthouden
* Tekenconventie: Werk is positief wanneer het systeem werkt op de omgeving (uitbreiding). Werk is negatief wanneer het werk aan het systeem wordt gedaan (compressie).
* Ideale gasaannames: Deze formules zijn gebaseerd op de ideale gaswet. In werkelijkheid kunnen echte gassen afwijken van deze uitdrukkingen.
* Toepassingen: Deze uitdrukkingen zijn van fundamenteel belang in de thermodynamica, vooral om te begrijpen hoe motoren en andere systemen werken.
Laat het me weten als je meer details wilt of specifieke scenario's hebt die je wilt verkennen!
Hoofdlijnen
- Welk type celdeling vindt plaats in alle cellen een organisme -lichaam behalve de reproductieve cellen?
- wat wordt bedoeld met trofische niveaus?
- Welke endocriene klier bevindt zich in de luchtpijp?
- Wat is homoloog in de evolutie?
- Welke van de volgende verklaringen verklaart het beste waarom soorten die zich seksueel voortplanten een voordeel hebben in een snel veranderende omgeving vergeleken met aseksueel?
- Hoe gelukkig te zijn in een relatie
- Wat is er een onafhankelijk of afzonderlijk bestaan?
- Wat wordt er weergegeven als geen enkele kopie van een allel de expressie maskeert?
- Biologen ontdekken hoe belangrijke mechanismen voor de aanhechting van koolhydraten niet goed werken
- Nieuwe zijden materialen kunnen kreuken in gedetailleerde patronen, dan ontkreuken om opnieuw te worden afgedrukt

- Simulaties laten zien hoe bèta-amyloïde neurale cellen kan doden

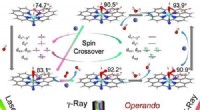
- Wetenschappers identificeren elektronische en structurele dynamiek van katalytische centra in materialen met één Fe-atoom
- Onderzoekslaboratoriumsimulator voltooit essentieel onderzoek naar geneesmiddelen in dagen

- Fluorescerend molecuul verraadt de afbraak van polymeermaterialen

 Welke planeet bevat het grootste deel van de massa in het zonnestelsel?
Welke planeet bevat het grootste deel van de massa in het zonnestelsel?  Splijting is het proces van het creëren van energie door?
Splijting is het proces van het creëren van energie door?  Wat verklaren de nevelvormige hypothisingen?
Wat verklaren de nevelvormige hypothisingen?  UCI, NASA onthult nieuwe details over ijsverlies in Groenland
UCI, NASA onthult nieuwe details over ijsverlies in Groenland Wat zorgt ervoor dat de sterren langzaam over de hemel bewegen in een zigzagpad?
Wat zorgt ervoor dat de sterren langzaam over de hemel bewegen in een zigzagpad?  Hoe zorgt mitose ervoor dat een nieuwe cel identiek is aan oudercel?
Hoe zorgt mitose ervoor dat een nieuwe cel identiek is aan oudercel?  Wat is de chemische samenstelling met een robijn?
Wat is de chemische samenstelling met een robijn?  De gematigde gletsjers in China smelten steeds sneller
De gematigde gletsjers in China smelten steeds sneller
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


