
Wetenschap
Wat is de relatie tussen reactanten en producten in een chemische vergelijking?
reactanten:
* startmaterialen: Dit zijn de stoffen die aanwezig zijn aan het begin van een chemische reactie.
* Transformatie ondergaan: Ze worden omgezet in nieuwe stoffen tijdens de reactie.
* aan de linkerkant: In een chemische vergelijking worden reactanten meestal aan de linkerkant van de pijl geschreven.
producten:
* resulterende stoffen: Dit zijn de stoffen die worden gevormd als gevolg van de chemische reactie.
* gemaakt door de reactie: Ze zijn gemaakt van de herschikking van atomen in de reactanten.
* aan de rechterkant gelegen: Producten worden meestal aan de rechterkant van de pijl geschreven in een chemische vergelijking.
Relatie:
* Transformatie: Reactanten worden omgezet in producten door chemische bindingen te doorbreken en te vormen.
* Behoud van massa: De totale massa van de reactanten moet gelijk zijn aan de totale massa van de producten. Dit is de wet van behoud van massa.
* stoichiometrie: De coëfficiënten in een evenwichtige chemische vergelijking vertegenwoordigen de relatieve hoeveelheden (mol) van reactanten en producten die bij de reactie betrokken zijn.
Voorbeeld:
Overweeg de verbranding van methaan:
ch₄ (g) + 2o₂ (g) → co₂ (g) + 2h₂o (g)
* reactanten: Methaan (ch₄) en zuurstof (o₂)
* Producten: Koolstofdioxide (CO₂) en water (H₂o)
In deze reactie reageren methaan en zuurstof om koolstofdioxide en water te vormen. De chemische bindingen in de reactanten zijn verbroken en nieuwe bindingen worden gevormd in de producten. Het aantal atomen van elk element blijft hetzelfde aan beide zijden van de vergelijking, wat de wet van behoud van massa aantoont.
Key Takeaways:
* Reactanten zijn de startmaterialen van een reactie en producten zijn de stoffen die hierdoor worden gevormd.
* De relatie tussen reactanten en producten is een transformatie aangedreven door het breken en vormen van chemische bindingen.
* De wet van behoud van massa regelt de relatie en zorgt ervoor dat massa niet wordt gecreëerd of vernietigd tijdens een chemische reactie.
 Soms kan waterdamp op een oppervlak bevriezen zonder eerst vloeibaar te worden. Wat ontstaat er als dit gebeurt?
Soms kan waterdamp op een oppervlak bevriezen zonder eerst vloeibaar te worden. Wat ontstaat er als dit gebeurt?  Wat is de chemische formule voor ironisch carbonaat?
Wat is de chemische formule voor ironisch carbonaat?  Wat is het dragermolecuul voor waterstof?
Wat is het dragermolecuul voor waterstof?  Wat zijn calcilicaat gneis?
Wat zijn calcilicaat gneis?  Afstemming van de elektrokatalytische prestaties van bifunctionele katalysatoren
Afstemming van de elektrokatalytische prestaties van bifunctionele katalysatoren
 Honderden vluchten vertraagd door mist die Noord-India overspoelt
Honderden vluchten vertraagd door mist die Noord-India overspoelt Hoe komt water in huizen, en wat gebeurt er nadat het is vertrokken? Hint:het is geen magie
Hoe komt water in huizen, en wat gebeurt er nadat het is vertrokken? Hint:het is geen magie Klimaatverandering kan de voedselketens in de oceaan veranderen, wat leidt tot veel minder vissen in de zee
Klimaatverandering kan de voedselketens in de oceaan veranderen, wat leidt tot veel minder vissen in de zee Wat bedoelde Darwin toen hij zei dat individuen moeite hebben om te overleven?
Wat bedoelde Darwin toen hij zei dat individuen moeite hebben om te overleven?  Kleine microben spelen een steeds grotere rol in de koolstofcyclus van de Chinese zeeën
Kleine microben spelen een steeds grotere rol in de koolstofcyclus van de Chinese zeeën
Hoofdlijnen
- Het samenvoegen van kernen en chromosomen is bekend als wat?
- Welk orgel pompt zuurstof en voedingsstoffen naar de weefsels van het lichaam?
- Wat zijn de 3 vormen van bacteriën en hun specifieke naam?
- Waarom groeit schimmels op fruit en brood?
- Vis vissen voor voedsel:Uit onderzoek blijkt dat de recreatieve visserij verantwoordelijk is voor 11% van de gerapporteerde oogst in de binnenvisserij
- Is de pijnappelklier lichtste orgel op het lichaam?
- Wat houdt in een cel de kern bij elkaar?
- Waar gaat de studie van de wetenschap over?
- Waarom wordt virus niet opgenomen in het micro -organisme?
- Medische zuurstof mag geen luxe zijn:een goedkopere manier ontwikkelen om het te produceren

- Wat moeten we doen met plastic voor eenmalig gebruik?

- Hoe lang duurt het geheugen? Voor legeringen met vormgeheugen, hoe langer hoe beter

- Nieuwe methode maakt de weg vrij voor snijgereedschappen met een langere levensduur

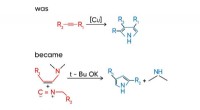
- Chemici stellen een nieuwe methode voor voor de synthese van pyrrolen
 Onderzoekers laten zien dat het buigen van halfgeleiders elektriciteit opwekt
Onderzoekers laten zien dat het buigen van halfgeleiders elektriciteit opwekt  Hoeveel AU is elke planeet van de zon?
Hoeveel AU is elke planeet van de zon?  Vergelijk en contrasteer de eigenschappen van vloeistoffen vaste stoffen?
Vergelijk en contrasteer de eigenschappen van vloeistoffen vaste stoffen?  Een oplossing met een hoge concentratie van niet-afnemende opgeloste stoffen wordt genoemd?
Een oplossing met een hoge concentratie van niet-afnemende opgeloste stoffen wordt genoemd?  Hoeveel centimeter zitten er in 1 diameter?
Hoeveel centimeter zitten er in 1 diameter?  Algoritme geeft robots een instinctief begrip van hoe ze tools moeten gebruiken
Algoritme geeft robots een instinctief begrip van hoe ze tools moeten gebruiken  Vallen voorwerpen met dezelfde snelheid vanwege hun massa?
Vallen voorwerpen met dezelfde snelheid vanwege hun massa?  Waarom stoppen bij plastic zakken en rietjes? Pleidooi voor een wereldwijd verdrag dat de meeste kunststoffen voor eenmalig gebruik verbiedt
Waarom stoppen bij plastic zakken en rietjes? Pleidooi voor een wereldwijd verdrag dat de meeste kunststoffen voor eenmalig gebruik verbiedt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

