
Wetenschap
Wat is de dichtheid van stikstof bij 100 psi?
Dit is waarom:
* Dichtheid is een functie van zowel druk als temperatuur. Hoe hoger de druk, hoe meer moleculen in een bepaald volume worden verpakt, waardoor de dichtheid toeneemt. Evenzo zorgt de hogere temperatuur ervoor dat moleculen sneller bewegen en zich verspreiden, waardoor de dichtheid afneemt.
* De ideale gaswet: Deze fundamentele wet relateert druk (P), volume (V), temperatuur (T) en het aantal mol (N) van een gas door de vergelijking:PV =NRT, waarbij R de ideale gasconstante is.
* Dichtheid (ρ) wordt berekend als massa (m) per volume -eenheid (v): ρ =m/v.
Om de stikstofdichtheid bij 100 psi te berekenen, moet u de temperatuur kennen:
1. Bekleed druk in atmosferen: 100 psi is ongeveer 6,8 atmosferen (1 atm =14,7 psi).
2. Gebruik de ideale gaswet om het molaire volume te vinden: U moet de vergelijking herschikken om op te lossen voor V/N.
3. Bereken de dichtheid: Met behulp van het molaire volume en de molaire stikstofmassa (28 g/mol) kunt u de dichtheid berekenen.
Voorbeeld:
Laten we zeggen dat de temperatuur 25 ° C (298 K) is:
1. Converteer de temperatuur naar Kelvin: T =25 ° C + 273.15 =298 K.
2. Bereken molaire volume: Met behulp van de ideale gaswetgeving, v/n =rt/p =(0,0821 l⋅atm/mol⋅K) (298 k)/(6,8 atm) ≈ 3,6 l/mol.
3. Bereken dichtheid: ρ =(28 g/mol)/(3,6 l/mol) ≈ 7,8 g/l.
Daarom is de dichtheid van stikstof bij 100 psi en 25 ° C ongeveer 7,8 g/l.
 Hoeveel Cl-ionen zijn er voor elk Na-ion in de formule?
Hoeveel Cl-ionen zijn er voor elk Na-ion in de formule?  Hoe kunnen metalen worden samengevoegd met behulp van het meeslepende en het bestrijdende proces?
Hoe kunnen metalen worden samengevoegd met behulp van het meeslepende en het bestrijdende proces?  Ingenieurs demonstreren supersterk, omkeerbare lijm die werkt als slakkenslijm (update)
Ingenieurs demonstreren supersterk, omkeerbare lijm die werkt als slakkenslijm (update) Wat is transparantie van zwavels?
Wat is transparantie van zwavels?  Hoe habanero-pepers reageren op stress
Hoe habanero-pepers reageren op stress
 Steenkool maken van voedselafval, tuinafval – en zelfs menselijk afvalwater
Steenkool maken van voedselafval, tuinafval – en zelfs menselijk afvalwater Koppeling aan tropische regenval en temperatuur van het zeeoppervlak kan de voorspellingen verbeteren
Koppeling aan tropische regenval en temperatuur van het zeeoppervlak kan de voorspellingen verbeteren Is er een onderscheid tussen lichte reflectie en breking?
Is er een onderscheid tussen lichte reflectie en breking?  Klimaatverandering vertraagt de Atlantische stromingen die Europa en de Atlantische kust verwarmen
Klimaatverandering vertraagt de Atlantische stromingen die Europa en de Atlantische kust verwarmen Heeft de klimaatchaos het groen van 2023 gecultiveerd of beperkt?
Heeft de klimaatchaos het groen van 2023 gecultiveerd of beperkt?
Hoofdlijnen
- Wat zijn de oorsprong van mensen met bloedgroep AB?
- Wat is de slogeen voor schaal?
- Hoeveel ATP-moleculen per glucose krijgt een cel bij elk van de drie stadia van cellulaire ademhaling?
- Het deel van de biosfeer rondom een organisme is het?
- Wetenschappers leren hoe ze het vermogen van microben om herinneringen te maken kunnen vergroten
- Hoe wordt de kloof tussen tanden van een herbivoor genoemd?
- Uit onderzoek blijkt hoe lichaamscellen in een weefsel bewegen
- Wat is de belangrijkste taak die micro -organismen doen?
- Wat is in een voedselketen of internet?
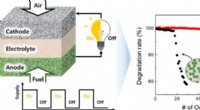
- Lager nikkelgehalte en verbeterde stabiliteit en prestaties in keramische brandstofcellen
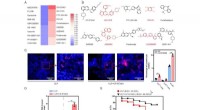
- PDGFR-kinaseremmer blijkt te beschermen tegen septische dood via regulering van BTLA
- Zelfmontage vereist:neutronen onderzoeken nieuw polymeergedrag voor biomedische materialen

- Drooggezouten hambotten - een bron van hart-gezonde peptiden?
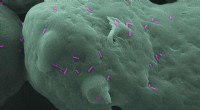
- Wetenschappers maken 3D-geprinte onderdelen die bacteriën kunnen doden
 Hoeveel radioactieve elementen worden er in het laboratorium gemaakt?
Hoeveel radioactieve elementen worden er in het laboratorium gemaakt?  Nieuwe antivirale, antibacterieel oppervlak kan de verspreiding van infecties in ziekenhuizen verminderen
Nieuwe antivirale, antibacterieel oppervlak kan de verspreiding van infecties in ziekenhuizen verminderen Wat is de snelheid die asteroïden reizen?
Wat is de snelheid die asteroïden reizen?  Onderzoekers stellen nieuwe ontwerpmethoden voor permanente magneten voor voor quasi-assymmetrische stellarator
Onderzoekers stellen nieuwe ontwerpmethoden voor permanente magneten voor voor quasi-assymmetrische stellarator Nieuwe studie onthult dat de meeste Europeanen het basisinkomen steunen na COVID-19
Nieuwe studie onthult dat de meeste Europeanen het basisinkomen steunen na COVID-19 Nieuwe selfie-microsatelliet legt beelden vast van Chinees ruimtestation
Nieuwe selfie-microsatelliet legt beelden vast van Chinees ruimtestation Waar kan men een Bose Sound Wave kopen?
Waar kan men een Bose Sound Wave kopen?  Amerikaanse klimaatsceptici doen rillingen over de Arctische samenwerking
Amerikaanse klimaatsceptici doen rillingen over de Arctische samenwerking
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

