
Wetenschap
Hebben niet -metalen of metalen een hoge thermische en elektrische geleidbaarheid?
Dit is waarom:
* gratis elektronen: Metalen hebben een unieke structuur waar hun buitenste elektronen losjes gebonden zijn en vrij door het materiaal kunnen bewegen. Deze "vrije elektronen" zijn de sleutel tot hun hoge geleidbaarheid.
* Thermische geleidbaarheid: Wanneer warmte op een metaal wordt aangebracht, absorberen deze vrije elektronen energie en bewegen snel rond, waardoor warmte door het materiaal wordt overgebracht.
* elektrische geleidbaarheid: Evenzo, wanneer een elektrisch veld wordt aangebracht, stromen de vrije elektronen gemakkelijk, waardoor een elektrische stroom ontstaat.
niet -metalen , aan de andere kant, hebben hun elektronen strak gebonden aan hun atomen. Dit maakt het moeilijk voor hen om vrij te bewegen, wat resulteert in een lage thermische en elektrische geleidbaarheid.
Uitzonderingen: Hoewel de meeste niet -metalen slechte geleiders zijn, zijn er enkele uitzonderingen:
* koolstof (in de vorm van grafiet) is een uitstekende geleider van elektriciteit vanwege de unieke gelaagde structuur die vrije elektronenbeweging mogelijk maakt.
* silicium en germanium zijn halfgeleiders, wat betekent dat ze geleidbaarheid hebben tussen metalen en niet -metalen. Ze zijn cruciaal in elektronica.
 Waarom uw tonijn 36 keer meer chemicaliën kan bevatten dan andere
Waarom uw tonijn 36 keer meer chemicaliën kan bevatten dan andere Gebroken gesteente in bossen wordt over het hoofd gezien als bron van natuurlijke koolstofdioxide
Gebroken gesteente in bossen wordt over het hoofd gezien als bron van natuurlijke koolstofdioxide Duitsland zindert in recordtemperaturen in juni
Duitsland zindert in recordtemperaturen in juni Het leerboek over fossiele brandstoffen herschrijven:nieuwe technologieën helpen de methaanrecepten van de natuur te ontrafelen
Het leerboek over fossiele brandstoffen herschrijven:nieuwe technologieën helpen de methaanrecepten van de natuur te ontrafelen Onderzoekers onthullen de mate waarin rivieren in het hele land stroom verliezen aan watervoerende lagen
Onderzoekers onthullen de mate waarin rivieren in het hele land stroom verliezen aan watervoerende lagen
Hoofdlijnen
- Eerste foto's van BRCA2-eiwit laten zien hoe het werkt om DNA te repareren
- Welke soorten genen hebben plasmiden?
- Hoe weet het lichaam wanneer hij nieuwe cellen moet maken?
- Wat is de relatie tussen het ademhalingsproces en de cellulaire ademhaling?
- Wat richt alle celactivites?
- Hoeveel chromosomen zitten er in een diploïde cel?
- Hoe belangrijk is dieronderzoek naar de medische wetenschap geweest?
- Moordende meerval? Giftige soorten die verrassend vaak voorkomen, blijkt uit onderzoek
- Wat eten leden van de Kingdom Fungi?
- Hoe robotwiskunde en smartphones onderzoekers naar een doorbraak in de ontdekking van medicijnen hebben geleid

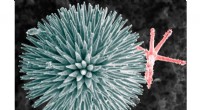
- Als je beter kijkt, zie je axiale filamenten in spicules van zeespons die uit eiwitten bestaan
- Een radicale oplossing komt van het mengen van gereedschappen

- Akoestische oplossingen gemaakt van natuurlijke vezels kunnen de ecologische voetafdruk van gebouwen verkleinen

- Wat maakt een rokerige, verkoolde barbecue zo lekker? De chemie van koken boven een open vuur

 Chimpansees:alarmoproepen met opzet?
Chimpansees:alarmoproepen met opzet?  Door de natuur geïnspireerde nanostructuren betekenen geen ramen meer schoonmaken
Door de natuur geïnspireerde nanostructuren betekenen geen ramen meer schoonmaken Krachtig nieuw apparaat voor het bestuderen van het puzzelproces
Krachtig nieuw apparaat voor het bestuderen van het puzzelproces Op hout gebaseerde vezels vangen hormonen uit afvalwater
Op hout gebaseerde vezels vangen hormonen uit afvalwater Machine learning kraakt de oxidatietoestanden van kristalstructuren
Machine learning kraakt de oxidatietoestanden van kristalstructuren Bouwstenen voor op RNA gebaseerd leven in het centrum van ons melkwegstelsel
Bouwstenen voor op RNA gebaseerd leven in het centrum van ons melkwegstelsel Golfgeleider met laag buigverlies opent de weg naar inkrimping van 3D fotonische geïntegreerde schakelingen
Golfgeleider met laag buigverlies opent de weg naar inkrimping van 3D fotonische geïntegreerde schakelingen Welke parasiet wordt vaak overgedragen van dieren op mensen door contact met vervuilde ontlasting?
Welke parasiet wordt vaak overgedragen van dieren op mensen door contact met vervuilde ontlasting?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

