
Wetenschap
Wat is de elektronenconfiguratie van fosfor?
De elektronenconfiguratie van fosfor is:
1S² 2S² 2P⁶ 3S² 3P³
Hier is een uitsplitsing:
* 1S²: Het eerste energieniveau (n =1) heeft twee elektronen in de 's' subshell.
* 2S²: Het tweede energieniveau (n =2) heeft twee elektronen in de 's' subshell.
* 2p⁶: Het tweede energieniveau (n =2) heeft zes elektronen in de 'P' subshell.
* 3S²: Het derde energieniveau (n =3) heeft twee elektronen in de 's' subshell.
* 3p³: Het derde energieniveau (n =3) heeft drie elektronen in de 'P' subshell.
Belangrijke opmerking: Dit is de elektronenconfiguratie van de grondtoestand. Fosfor kan ook bestaan in geëxciteerde toestanden waar elektronen hogere energieniveaus bezetten.
 Is fluor het meest reactieve element bij halogeenfamilie.
Is fluor het meest reactieve element bij halogeenfamilie.  Wat is de studie van elementen. atomen. en moleculen gebeld?
Wat is de studie van elementen. atomen. en moleculen gebeld?  Na het koken, bioversterkte maïs en eieren behouden de voedingsstoffen die nodig zijn om blindheid te voorkomen
Na het koken, bioversterkte maïs en eieren behouden de voedingsstoffen die nodig zijn om blindheid te voorkomen Eerste gedetailleerde blik op cruciaal enzym bevordert kankeronderzoek
Eerste gedetailleerde blik op cruciaal enzym bevordert kankeronderzoek De chemicaliën in zout, peper & suiker
De chemicaliën in zout, peper & suiker
Hoofdlijnen
- Waarom subfylum filicinophyta sp meer vooruitgang thansubphylum lycopodiophyta sp?
- Ingenieurs hacken celbiologie om 3D-vormen te maken van levend weefsel
- Wat is een epidermis?
- Wat is de naam van het proces dat eindproduct ATP?
- Waarom hebben cellen een klein oppervlak?
- Is het Ida-fossiel de ontbrekende schakel?
- Wat zou een wetenschapper doen als de gemeenschappelijke theorieën niet van toepassing zijn op bevindingen van zijn of haar werk?
- Mitosis vs Meiosis: Wat zijn de overeenkomsten en verschillen?
- Wat is het plantengedeelte dat wordt gevormd door een succesvolle vereniging van mannelijke pollencel en vrouwelijke eicel, draagt dus kenmerken van beide ouders?
- Kleurrijke oplossing voor een knelpunt in de chemische industrie

- Ondersteuning stuurt het lot van beschermde gouden nanoclusters als katalysatoren

- Nieuwe techniek waarbij medicijnen bacteriën laten gloeien, kan antibioticaresistentie helpen bestrijden
- DNA-origami veerkrachtiger dan eerder werd begrepen

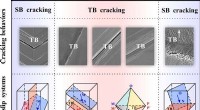
- Kunnen tweelinggrenzen bestand zijn tegen vermoeiingsscheuren?
 Welke twee hoofdprocessen waarmee plantencellen afgifte absorberen en energie gebruiken?
Welke twee hoofdprocessen waarmee plantencellen afgifte absorberen en energie gebruiken?  Welk minerale functie ontstaat en wordt groter met toenemend metamorfisme?
Welk minerale functie ontstaat en wordt groter met toenemend metamorfisme?  Cape of Storms:Klimaatonderzoekers verklaren het recente extreme weer in Kaapstad
Cape of Storms:Klimaatonderzoekers verklaren het recente extreme weer in Kaapstad  Het aantal neutronen, protonen en elektronen voor atomen, ionen en isotopen vinden
Het aantal neutronen, protonen en elektronen voor atomen, ionen en isotopen vinden Een opgeblazen ballon wordt een hoge berg gedragen, zal het groter of kleiner worden, uitleggen waarom het volume verandert?
Een opgeblazen ballon wordt een hoge berg gedragen, zal het groter of kleiner worden, uitleggen waarom het volume verandert?  Interacties in designermaterialen onthuld
Interacties in designermaterialen onthuld JWST-gegevens suggereren dat exoplaneet K2-18b mogelijk een gesmolten oppervlak heeft in plaats van een waterige oceaan
JWST-gegevens suggereren dat exoplaneet K2-18b mogelijk een gesmolten oppervlak heeft in plaats van een waterige oceaan  Hoe het interieur van de aarde is verdeeld in lagen?
Hoe het interieur van de aarde is verdeeld in lagen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

