
Wetenschap
Covalente verbindingen tonen welke van deze eigenschappen?
Algemene eigenschappen:
* Laag smelt- en kookpunten: In vergelijking met ionische verbindingen hebben covalente verbindingen over het algemeen zwakkere intermoleculaire krachten (krachten tussen moleculen), wat leidt tot lagere smelt- en kookpunten.
* Slechte elektrische geleidbaarheid: Covalente verbindingen zijn over het algemeen slechte geleiders van elektriciteit in zowel vaste als vloeibare toestanden omdat ze geen vrij bewegende geladen deeltjes (ionen) hebben.
* Oplosbaarheid in niet-polaire oplosmiddelen: Covalente verbindingen, vooral die met niet-polaire bindingen, hebben de neiging om op te lossen in niet-polaire oplosmiddelen zoals koolwaterstoffen.
* bestaan vaak als gassen of vloeistoffen bij kamertemperatuur: Vanwege hun zwakkere intermoleculaire krachten zijn veel covalente verbindingen gassen of vloeistoffen bij kamertemperatuur.
Specifieke eigenschappen:
* Sterke intramoleculaire bindingen: Covalente verbindingen hebben sterke bindingen in het molecuul (covalente bindingen), maar zwakkere intermoleculaire krachten tussen moleculen.
* Variabele smelten en kookpunten: Hoewel in het algemeen lager, kunnen de smelt- en kookpunten sterk variëren, afhankelijk van de grootte en complexiteit van de moleculen.
* kan vaste stoffen, vloeistoffen of gassen zijn: De fysieke toestand bij kamertemperatuur hangt af van de sterkte van intermoleculaire krachten.
* kan ontvlambaar zijn: Sommige covalente verbindingen zijn zeer ontvlambaar, vooral die met koolstof en waterstof (koolwaterstoffen).
* variabele reactiviteit: De reactiviteit van covalente verbindingen hangt af van de specifieke betrokken elementen en de soorten aanwezige bindingen.
Voorbeelden:
* water (h₂o): Een vloeistof bij kamertemperatuur, goed oplosmiddel voor polaire moleculen, maar een slechte geleider van elektriciteit.
* methaan (ch₄): Een gas bij kamertemperatuur, ontvlambaar, niet-polair en oplosbaar in niet-polaire oplosmiddelen.
* suiker (c₁₂h₂₂o₁₁): Een vaste stof bij kamertemperatuur, oplosbaar in water, niet-geleider van elektriciteit.
Laat het me weten als u een meer gedetailleerde uitleg van een specifieke eigenschap wilt!
 Nieuwe gepatenteerde technologie verwijdert fosfor uit mest
Nieuwe gepatenteerde technologie verwijdert fosfor uit mest Hoe fotografie van plaats delict werkt
Hoe fotografie van plaats delict werkt  Een dicht netwerk van seismometers laat zien hoe de ondergrond scheurt
Een dicht netwerk van seismometers laat zien hoe de ondergrond scheurt  Warmere temperaturen veroorzaken een afname van de belangrijkste afvoermaatregel
Warmere temperaturen veroorzaken een afname van de belangrijkste afvoermaatregel Experimenten voor de binnenluchtkwaliteit tonen blootstellingsrisico's aan tijdens het koken, schoonmaken
Experimenten voor de binnenluchtkwaliteit tonen blootstellingsrisico's aan tijdens het koken, schoonmaken
Hoofdlijnen
- Voor fotosynthese heeft een cel wat 3 dingen nodig?
- Wat is de elektrische impuls die een Axon naar beneden beweegt?
- Waarom sterft de evolutie?
- Wat is osmose in termen van waterpotentieel?
- Waarom fokken in gevangenschap de wilde tijger niet zal redden
- Wat betekent generatietijd in de microbiologie?
- Wat regelt de doorgang van voedingsstoffen in cel en verspilt cel?
- Wat zou er gebeuren als een cel geen ribosomen zou hebben?
- Wat is geen proces dat deel uitmaakt van de moderne laboratoriumgenetica?
- Nieuwe explosieve materialen om niet-giftige munitie mee te nemen

- Chemicus ontwikkelt techniek om zonnecellen te verbeteren
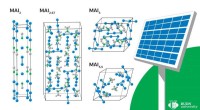
- Een molecuul dat werkt als een nanobatterij

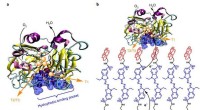
- Verbetering van de elektronenoverdracht in enzymatische biobrandstofcellen
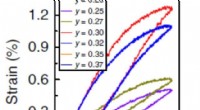
- Nieuw keramisch materiaal kan de kosten van piëzo-elektrische apparaten verlagen
 Welke energie wint een lift als deze omhoog gaat?
Welke energie wint een lift als deze omhoog gaat?  Natuurkundigen gebruiken computersimulatie om veroudering in levende glasachtige systemen te onderzoeken
Natuurkundigen gebruiken computersimulatie om veroudering in levende glasachtige systemen te onderzoeken Waar of niet waar als een stof verbrandt, is destally?
Waar of niet waar als een stof verbrandt, is destally?  Welke warmteoverdracht is in vaste stoffen?
Welke warmteoverdracht is in vaste stoffen?  Waarom moeten mensen wetenschapsexperimenten?
Waarom moeten mensen wetenschapsexperimenten?  All-photonic quantum repeaters kunnen leiden tot een snellere, veiliger wereldwijd kwantuminternet
All-photonic quantum repeaters kunnen leiden tot een snellere, veiliger wereldwijd kwantuminternet Zwembacteriën werken samen om met de stroom mee te gaan
Zwembacteriën werken samen om met de stroom mee te gaan Met zeep betrapt:begrijpen hoe zeepmoleculen eiwitten helpen om in en uit vorm te komen
Met zeep betrapt:begrijpen hoe zeepmoleculen eiwitten helpen om in en uit vorm te komen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

