
Wetenschap
Wat is de lading op koolstofatoom in methylamine?
Dit is waarom:
* elektronegativiteit: Stikstof is elektronegatiefer dan koolstof. Dit betekent dat stikstof elektronen sterker aantrekt in de C-N-binding.
* Elektronendichtheid: Als gevolg hiervan wordt de elektronendichtheid in de C-N-binding verschoven naar het stikstofatoom, waardoor het koolstofatoom enigszins elektronenrijk is.
* Formele lading: Hoewel geen echte lading, is de formele lading op koolstof in methylamine 0. Het verschil van elektronegativiteit creëert echter een gedeeltelijke negatieve lading op het koolstofatoom.
Daarom heeft het koolstofatoom in methylamine een gedeeltelijke negatieve lading, die wordt geschat op ongeveer -0,3.
 Impact van grote vulkaanuitbarstingen in de afgelopen twee millennia op zowel het mondiale als het Chinese klimaat
Impact van grote vulkaanuitbarstingen in de afgelopen twee millennia op zowel het mondiale als het Chinese klimaat  NASA analyseert de nieuwste subtropische depressie in de Atlantische Oceaan
NASA analyseert de nieuwste subtropische depressie in de Atlantische Oceaan Onderwaterverdediging:nieuwe manieren om duikers in de diepte te beschermen
Onderwaterverdediging:nieuwe manieren om duikers in de diepte te beschermen Na de bosbranden hielpen we bij het uitkiezen van de dieren en planten die het meest nodig waren. Hier is hoe het gebeurde
Na de bosbranden hielpen we bij het uitkiezen van de dieren en planten die het meest nodig waren. Hier is hoe het gebeurde  Het ontsluiten van de klimaatgeheimen van Noord-China met eeuwenoude boomringen
Het ontsluiten van de klimaatgeheimen van Noord-China met eeuwenoude boomringen
Hoofdlijnen
- Welke rol speelt cytokinese tijdens de celcyclus?
- Welke cytoskeletale eiwitten zijn belangrijke bestanddelen van de contractiele structuren die splitsing vormen die betrokken zijn bij cytokinese van diercellen?
- Wat zijn de snelheidsbeperkende enzymen voor het ATP-PC-systeem?
- Wat zijn de verschillen tussen suikers en bases van nucleotide -DNA -RNA?
- Welk organisme studeerde Charles Darwin?
- Is het ribosoom een plantaardige of dierlijke structuur?
- Wat is de rol van enzymen bij biologisch wassen?
- Is het verschil tussen glycogeen en zetmeel?
- Dikke eekhoorn steelt dure goederen die zijn achtergelaten voor bezorgers
- Nooit meer met vuur spelen:onderzoek biedt inzicht in veiligere oplaadbare batterijen

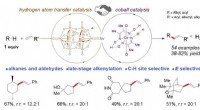
- Nieuwe methode voor functionalisering van koolstof-waterstofbindingen in een laat stadium
- Studie beschrijft cellulaire fabrieken in meer detail
- Onderzoekers testen cellen met siliciumanoden, aluminiumoxide coatings die kathoden beschermen

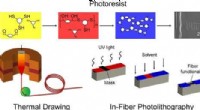
- Patterning-methode kan de weg vrijmaken voor nieuwe op glasvezel gebaseerde apparaten, slim textiel
 Neutronenexperimenten automatiseren met AI
Neutronenexperimenten automatiseren met AI Hoe NASA Europa Clipper beschermt tegen ruimtestraling
Hoe NASA Europa Clipper beschermt tegen ruimtestraling  Welk landvorm heeft een vlak land met steile zijden?
Welk landvorm heeft een vlak land met steile zijden?  Satellietgegevens geleide inspanning om Nepal te helpen herstellen van een reeks aardbevingen
Satellietgegevens geleide inspanning om Nepal te helpen herstellen van een reeks aardbevingen Hoe het genoom is verpakt in chromosomen die getrouw kunnen worden verplaatst tijdens celdeling
Hoe het genoom is verpakt in chromosomen die getrouw kunnen worden verplaatst tijdens celdeling  Schrijf de chemische reactie tussen cyclopenteen en kaliumpermanganaat?
Schrijf de chemische reactie tussen cyclopenteen en kaliumpermanganaat?  Waarom is lichaamstemperatuur niet goed vastgesteld voor het opzetten van schaal?
Waarom is lichaamstemperatuur niet goed vastgesteld voor het opzetten van schaal?  Astronauten knijpen in laatste ruimtewandeling voor vertrek SpaceX
Astronauten knijpen in laatste ruimtewandeling voor vertrek SpaceX
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

