
Wetenschap
Waarom is zwaveltrioxide niet direct in water opgelost om zuur te krijgen?
Dit is waarom:
* exotherme reactie: Wanneer zo oplost in water, vormt het zwavelzuur in een sterk exotherme reactie. De gegenereerde warmte kan ervoor zorgen dat het water gewelddadig kookt, waardoor spatten en brandwonden mogelijk worden veroorzaakt.
* Vorming van zwavelzuur mist: De vrijgegeven warmte kan er ook voor zorgen dat een deel van het zwavelzuur verdampt, waardoor een corrosieve mist wordt gevormd die gevaarlijk is om te inademen.
* veiligheidsproblemen: Directe oplossing van SO₃ in water wordt als zeer gevaarlijk beschouwd en is geen veilige of praktische manier om zwavelzuur te produceren.
In plaats daarvan wordt een veiliger en meer gecontroleerde methode gebruikt:
* absorptie in geconcentreerd zwavelzuur: Dus ₃ wordt eerst opgelost in geconcentreerd zwavelzuur, waardoor oleum wordt geproduceerd , wat in wezen een oplossing is van SO₃ in H₂so₄. Dit proces is minder exotherme en veiliger.
* verdunning met water: Het oleum wordt vervolgens zorgvuldig verdund met water, waardoor de SO₃ op een gecontroleerde manier kan reageren met water om H₂so₄ te vormen.
Deze methode zorgt ervoor dat de gegenereerde warmte effectief wordt beheerd, waardoor potentiële gevaren worden voorkomen.
Daarom wordt direct oplost dat zo ₃ in water wordt vermeden vanwege de exotherme aard van de reactie en de veiligheidsproblemen die het vormt.
 Wanneer vloeibaar zilvernitraat en natriumchloride worden gecombineerd vaste vormen samen met een nieuw nitraat. Welke stof vertegenwoordigt het neerslag?
Wanneer vloeibaar zilvernitraat en natriumchloride worden gecombineerd vaste vormen samen met een nieuw nitraat. Welke stof vertegenwoordigt het neerslag?  Waarom is water een betere geleider dan ethanol?
Waarom is water een betere geleider dan ethanol?  Waarom komen nucleaire reacties op?
Waarom komen nucleaire reacties op?  De weg vrijmaken voor zuinige meststoffen
De weg vrijmaken voor zuinige meststoffen Welke reactanten is nodig voor een verbrandingsreactie?
Welke reactanten is nodig voor een verbrandingsreactie?
 Elektrogeochemie legt koolstof vast, produceert brandstof, compenseert verzuring van de oceaan
Elektrogeochemie legt koolstof vast, produceert brandstof, compenseert verzuring van de oceaan Welke plant zal de helderste in de lucht zijn?
Welke plant zal de helderste in de lucht zijn?  Een Amerikaans bureau onderzoekt hoe uitbraken van algenbloei kunnen worden opgespoord
Een Amerikaans bureau onderzoekt hoe uitbraken van algenbloei kunnen worden opgespoord  Venetië is overstroomd, maar andere steden zijn in veel groter gevaar
Venetië is overstroomd, maar andere steden zijn in veel groter gevaar Welke soorten vissen eten Eendekroos?
Welke soorten vissen eten Eendekroos?
Hoofdlijnen
- Levens in evenwicht:waarom houden we vast aan potentieel schadelijke, ziekteverwekkende mutaties?
- Toezicht op abortus bij vee zou het levensonderhoud kunnen beschermen en opkomende mondiale ziekteverwekkers kunnen opsporen
- Wat voor soort bladvenatie heeft Coriander?
- Wat was er eerst:het hoofd of de hersenen?
- Wat is het verschil tussen een wetenschapper en onderzoeker?
- Wat zijn de basisbehoeften van organismen?
- Welke basis ontbreekt op RNA en welke andere vervangt het?
- Waar worden lipiden gesynthetiseerd in eukaryoten?
- Welk type epitheelweefsel is aanwezig in de organen waar uitwisselingsstoffen plaatsvinden?
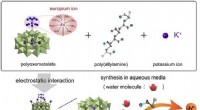
- Hybride materiaal brengt transportbrandstofcellen van de volgende generatie dichterbij
- Biosensor maakt realtime zuurstofmonitoring mogelijk voor organen-op-een-chip

- Nieuw onderzoek naar biofilms kan leiden tot een duurzamere waterindustrie

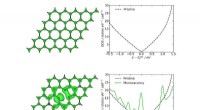
- Defect grafeen heeft een hoge elektrokatalytische activiteit
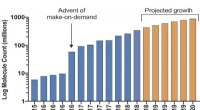
- Mega docking-bibliotheek klaar om de ontdekking van medicijnen te versnellen
 Effecten van ijstijden uit het verleden wijdverbreid dan eerder werd gedacht
Effecten van ijstijden uit het verleden wijdverbreid dan eerder werd gedacht Wetenschappers ontdekken de grootste zeewierbloei ter wereld
Wetenschappers ontdekken de grootste zeewierbloei ter wereld Hoe gebruik je Caustic Soda Flakes?
Hoe gebruik je Caustic Soda Flakes?  Onderzoekers herontdekken snelwerkend Duits insecticide dat verloren was gegaan in de nasleep van de Tweede Wereldoorlog
Onderzoekers herontdekken snelwerkend Duits insecticide dat verloren was gegaan in de nasleep van de Tweede Wereldoorlog Om vliegtuigen on-the-fly te ontdooien, onderzoekers streven ernaar ijsvorming te beheersen in plaats van te bestrijden
Om vliegtuigen on-the-fly te ontdooien, onderzoekers streven ernaar ijsvorming te beheersen in plaats van te bestrijden Musk-geregeerde Twitter:gebruikers over om trollen en verkeerde informatie te bestrijden?
Musk-geregeerde Twitter:gebruikers over om trollen en verkeerde informatie te bestrijden? Hoe seismometers het luiden van kerkklokken registreren
Hoe seismometers het luiden van kerkklokken registreren De aardkorst is gemaakt van?
De aardkorst is gemaakt van?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

